Вопросы эффективности и безопасности применения препаратов гормона роста в педиатрической практике | #03/17
Применение препаратов гормона роста (ГР) в терапевтических алгоритмах заболеваний, сопровождающихся нарушениями динамики ростовых показателей, сегодня обусловлено широкой доступностью несмотря на высокую стоимость. Рекомбинантный человеческий ГР, полученный биосинтетическим путем, используют в педиатрической практике как средство стимуляции роста, так и как метаболический регулятор нарушенных обменных процессов начиная с 1985 г. Вместе с тем препараты соматропина (МНН препаратов гормона роста) имеют определенные показания с доказанной эффективностью. Основным показанием к назначению соматропина является гипопитуитаризм. Именно лечение недостаточности ГР при гипопитуитаризме препаратами соматропина является патогенетически обоснованным и проводится с заместительной целью.
Применение ГР при других вариантах низкорослости возможно, но прогностически непредсказуемо. К настоящему времени имеются данные об эффективности лечения ГР детей с внутриутробной задержкой роста, семейной низкорослостью, синдромами Шерешевского–Тернера, Прадера–Вилли, Рассела–Сильвера, анемией Фанкони, гликогенозом, хронической почечной недостаточностью, скелетными дисплазиями, муковисцидозом [1].
К настоящему времени имеются данные об эффективности лечения ГР детей с внутриутробной задержкой роста, семейной низкорослостью, синдромами Шерешевского–Тернера, Прадера–Вилли, Рассела–Сильвера, анемией Фанкони, гликогенозом, хронической почечной недостаточностью, скелетными дисплазиями, муковисцидозом [1].
С 2003 г. в США используют биосинтетический ГР для лечения детей с идиопатической низкорослостью. Возраст в начале терапии ГР и ответ на терапию ГР в первый год лечения являются основными факторами, определяющими конечный рост при идиопатической низкорослости. Предполагалось, что дети с хорошим ростовым ответом в первый год лечения ГР при идиопатической низкорослости скорее всего будут иметь хороший конечный рост при использовании даже низких доз ГР [2]. Однако результаты наблюдения показали, что индивидуальный эффект терапии остается сложным для предсказания. Большая вариабельность ауксиологических данных, возраст, показатели роста и костного возраста на момент начала терапии, скорость роста в первый год лечения определяют многофакторный анализ, сложный для прогнозирования.
Достаточно сложно прогнозировать ответ на лечение ГР также и при заместительной терапии. Оценка эффективности лечения ГР при соматотропной недостаточности по ауксиологическим параметрам показала, что ростовой ответ является переменным и различен в каждом конкретном случае [3]. Характерной особенностью терапии соматотропной недостаточности является то, что по данным наблюдений за терапией пациентов результат первого года лечения выше, чем в последующие годы. При этом отмечено, что единственным клинически значимым предиктором ответа роста на начало лечения в первый год является возраст начала терапии. Тогда как ни пик ГР при проведении стимуляционных тестов, ни пол, ни рост на момент начала терапии, индекс массы тела (ИМТ), костный возраст, доза ГР не влияют на скорость роста в первый год терапии. Более ранняя диагностика и лечение ГР позволяют достичь лучшего конечного роста в тяжелых случаях недостаточности ГР. Показано, что лучший ответ на лечение отмечался у детей с тяжелой степенью недостаточности ГР [4]. Но, по другим данным, конечный рост не имеет существенных различий у пациентов с тяжелым дефицитом ГР и пациентов с парциальным дефицитом ГР [5].
Но, по другим данным, конечный рост не имеет существенных различий у пациентов с тяжелым дефицитом ГР и пациентов с парциальным дефицитом ГР [5].
Рядом исследований было показано, что рост родителей является одним из показателей, который позволяет прогнозировать конечный рост у пациентов с дефицитом ГР, получающих заместительную терапию ГР. Было отмечено, что лечение ГР имеет лучшую эффективность у пациентов, в семьях которых не было родственников с низкорослостью [6].
Хотя лечение препаратами ГР не всегда сопровождается достижением генетически детерминированного роста, увеличение роста в первый год лечения в возрасте до начала полового развития коррелирует с общей прибавкой в росте при терапии. Это подтверждает важность начала лечения до начала пубертата [7].
В настоящее время ведется ряд исследований, с помощью которых подбирается необходимое сочетание лекарственных препаратов, комбинация с которыми ГР улучшит результаты лечения. Так, было показано, что одновременное назначение при врожденном дефиците ГР заместительной терапии ГР и агониста гонадолиберина с целью торможения инициации полового развития не имеет преимуществ перед назначением только ГР [8].
Ростовые эффекты ГР при соматотропной недостаточности у пациентов и с изолированным дефицитом ГР, и у пациентов с множественной недостаточностью гормонов гипофиза выражены с одинаковой степенью: 89% пациентов с изолированной недостаточностью ГР и 81% пациентов при множественном дефиците гормонов гипофиза достигают прогнозируемого роста. Причем бо?льшая прибавка в росте наблюдается в возрасте до начала пубертата [9].
Многолетний опыт лечения препаратами ГР показал, что лечение детей с низкорослостью с использованием дозы соматропина, рассчитанной на массу тела ребенка, сопровождается большой вариабельностью в ростовом ответе на терапию ГР. Вопрос, почему дети с недостаточностью ГР, терапия которых направлена на простое замещение недостающего ГР, имеют такие различные клинические исходы, до настоящего времени не решен.
Ведутся исследования, направленные на поиск фармакогеномных маркеров с прогностической значимостью чувствительности клеток к ГР.
Изучено изменение уровня инсулиноподобного фактора роста 1 (ИФР-1) после 1 месяца лечения ГР у детей с недостаточностью ГР и доказано, что имеется зависимость между полиморфизмом клеточного регулятора CDK4 и степенью изменения концентрации ИФР-1. Дальнейшее изучение взаимосвязи геномных маркеров и ранних изменений уровня ИФР-1 может позволить разработать стратегию быстрого индивидуального подбора дозы ГР при врожденной соматотропной недостаточности [10].
Дальнейшее изучение взаимосвязи геномных маркеров и ранних изменений уровня ИФР-1 может позволить разработать стратегию быстрого индивидуального подбора дозы ГР при врожденной соматотропной недостаточности [10].
Также на конечный рост пациентов, получающих лечение ГР, оказывает влияние наличие или отсутствие полиморфизма SOCS2 (rs3782415). Полиморфизм, выявляемый в GHR, IGFBP3 и SOCS2 локусах, влияет на результаты роста пациентов с врожденной соматотропной недостаточностью, получающих ГР. Использование этих генетических маркеров может определить пациентов, генетически предрасположенных к менее результативному лечению [11].
Конечным результатом подобных исследований должно стать признание важности индивидуального дозирования ГР для каждого пациента на основе конкретных индивидуальных геномных характеристик. Это позволит значительно улучшить терапию, которая в течение долгих лет базируется на принципе «одна дозировка подходит всем».
Насколько терапевтическая эффективность соматропина сопоставима с его безопасностью — вопрос, требующий глубокого детального анализа, решение которого возможно путем накопления опыта применения ГР при лечении различных форм низкорослости.
Безопасность во время лечения и неблагоприятные эффекты лечения ГР тщательно отслеживаются и описываются у детей с дефицитом ГР (как с изолированной, так и с множественной недостаточностью гормонов аденогипофиза) и у детей с идиопатической низкорослостью [12]. Согласно имеющейся информации, полученной в основном из постмаркетинговых исследований, поддерживаемых производителями препаратов ГР, имеется низкая частота (менее 3% пролеченных детей) побочных эффектов и увеличение благоприятного профиля безопасности ГР. Тем не менее, полный спектр потенциальных побочных эффектов ГР не точно диагностируется при помощи постмаркетинговых исследований. Это связано с достаточно длительным сроком лечения, меняющимися в динамике характеристиками больного и невозможностью отследить нежелательные явления после окончания лечения пациента [13–15].
Редко возникающим нежелательным явлением при лечении ГР является внутричерепная гипертензия. Более высокий риск ее развития отмечен в группах больных с хронической почечной недостаточностью, синдромом Шерешевского–Тернера и с органическими причинами дефицита ГР. Внутричерепная гипертензия обычно развивается в начальном периоде лечения или при увеличении дозы препаратов соматропина, прекращается с окончанием терапии ГР. Показанием для проведения фундоскопии офтальмологом являются симптомы, указывающие на внутричерепную гипертензию, такие как сильная головная боль, двоение/нечеткое зрение и рвота. Лечение часто может быть возобновлено при более низких дозах ГР без возврата симптомов.
Внутричерепная гипертензия обычно развивается в начальном периоде лечения или при увеличении дозы препаратов соматропина, прекращается с окончанием терапии ГР. Показанием для проведения фундоскопии офтальмологом являются симптомы, указывающие на внутричерепную гипертензию, такие как сильная головная боль, двоение/нечеткое зрение и рвота. Лечение часто может быть возобновлено при более низких дозах ГР без возврата симптомов.
К осложнениям терапии соматропином относят изменения в костной системе — эпифизеолиз и сколиоз. Эпифизеолиз диагностируется с частотой 73 на 100 000 лет лечения и встречается реже у больных с изолированным дефицитом ГР и идиопатической низкорослостью по сравнению с теми пациентами, у которых дефицит ГР наблюдается вследствие внутричерепных новообразований, краниофарингеомы [16]. Средняя продолжительность от начала терапии ГР до появления эпифизеолиза колеблется от 0,4 до 2,5 лет. Рекомендовано регулярное наблюдение за появлением соответствующих симптомов, таких как боли в бедре и/или боли в колене, изменения в походке, в случае положительного результата — тщательное обследование и консультация ортопеда. Эпифизеолиз требует хирургического вмешательства на эпифизе бедренной кости.
Эпифизеолиз требует хирургического вмешательства на эпифизе бедренной кости.
Сколиоз прогрессирует во время лечения ГР из-за быстрого роста, а не является прямым побочным эффектом ГР. Наиболее часто сколиоз развивается при лечении синдромальных форм низкорослости (например, при синдроме Шерешевского–Тернера и синдроме Прадера–Вилли) [17]. У 0,2% детей с идиопатической низкорослостью или с изолированным дефицитом ГР, получавших ГР, отмечено прогрессирование сколиоза [18]. Регулярное обследование на предмет наличия или прогрессирования сколиоза рекомендуется всем пациентам, получающим препараты ГР.
Данные научных публикаций и собственный практический клинический опыт свидетельствуют о необходимости мониторинга показателей метаболизма глюкозы у пациентов, получающих ГР. Это связано с доказанным фактом наличия резистентности к инсулину при лечении препаратами соматропина. Заболеваемость сахарным диабетом (СД) 1-го типа не увеличивается при терапии ГР. Вместе с тем известно, что больные с синдромом Шерешевского–Тернера, Прадера–Вилли имеют высокий риск развития неиммунных форм сахарного диабета. Снижение чувствительности к инсулину и компенсаторное увеличение секреции инсулина с обеспечением эугликемии сопровождается нарушением толерантности к глюкозе и требует коррекции метаболических нарушений, а в ряде случаев отмены препаратов ГР [19]. Мониторинг потенциального развития сахарного диабета с тестированием крови на уровень глюкозы и/или HbA1c должен быть включен в алгоритм наблюдения за всеми пациентами, получающими препараты ГР.
Снижение чувствительности к инсулину и компенсаторное увеличение секреции инсулина с обеспечением эугликемии сопровождается нарушением толерантности к глюкозе и требует коррекции метаболических нарушений, а в ряде случаев отмены препаратов ГР [19]. Мониторинг потенциального развития сахарного диабета с тестированием крови на уровень глюкозы и/или HbA1c должен быть включен в алгоритм наблюдения за всеми пациентами, получающими препараты ГР.
Патофизиологические и эпидемиологические наблюдения позволяют выразить опасение, что ГР может увеличить риск развития злокачественной опухоли во время или после терапии. Известно, что реализация ростового эффекта ГР опосредована соматомединами, один из которых ИФР-1. ИФР-1 и ГР относятся к веществам с митогенной и антиапоптозной активностью, и их рецепторы обнаружены в опухолях. Состояния нарушенной и избыточной секреции/действия ГР ассоциированы со снижением и повышением риска злокачественности соответственно. Снижение ИФР-1 через ограничение калорийности индуцирует апоптоз и предотвращает или замедляет рост опухоли [20–22]. Некоторые немногочисленные эпидемиологические исследования соотносят увеличение ГР и уровни ИФР-1 с опухолями толстой кишки, молочной железы, щитовидной железы и раком предстательной железы у взрослых [23]. В целом данные литературы указывают на разрешающую/факультативную, а не причинную роль ГР в онкогенезе.
Некоторые немногочисленные эпидемиологические исследования соотносят увеличение ГР и уровни ИФР-1 с опухолями толстой кишки, молочной железы, щитовидной железы и раком предстательной железы у взрослых [23]. В целом данные литературы указывают на разрешающую/факультативную, а не причинную роль ГР в онкогенезе.
Заболеваемость впервые выявленными во время лечения лейкемией или злокачественными новообразованиями в целом после лечения у детей без сопутствующих факторов риска не увеличивается по сравнению с таковой в общей популяции. Несмотря на данные об отсутствии влияния ГР на появление второго новообразования у детей, в анамнезе которых была неоплазия [24, 25], пункт о повышенном риске развития второго новообразования у пациентов, получавших ГР, в настоящее время присутствует в инструкции по применению на всех препаратах ГР в США. Отсутствуют данные относительно эффектов ГР на риск развития неоплазии у больных с заболеваниями, которые сами отнесены в группу повышенного риска возникновения новообразований. Риск новообразований у пациентов, получающих лечение ГР, был рассмотрен Комитетом по лекарственным средствам и терапии Общества детских эндокринологов, и ключевой рекомендацией является необходимость продолжающегося наблюдения всех пациентов, получавших лечение ГР, и это имеет первостепенное значение [26].
Риск новообразований у пациентов, получающих лечение ГР, был рассмотрен Комитетом по лекарственным средствам и терапии Общества детских эндокринологов, и ключевой рекомендацией является необходимость продолжающегося наблюдения всех пациентов, получавших лечение ГР, и это имеет первостепенное значение [26].
Перед началом терапии ребенка препаратами гормона роста его родители должны быть информированы о неопределенности в отношении долгосрочной безопасности (о неблагоприятных эффектах после терапии в зрелом возрасте).
Долгосрочные исследования (в среднем 17 лет) по наблюдению 6928 детей с изолированной соматотропной недостаточностью идиопатической низкорослостью, или низким гестационным возрастом, которые начали лечение ГР в период между 1985 и 1996 гг., во Франции показали 30%-й рост общей смертности по сравнению с населением в целом [27]. Все виды смертности, связанной с раком, не были увеличены, но стандартизованные показатели смертности были повышены в группах больных с опухолями костной системы, больных с нарушениями в системе кровообращения и больных с кровоизлиянием в мозг. Применение дозы препаратов ГР более 50 мкг/кг/день не рекомендовано. Полученные из той же базы данные в недавнем исследовании показали значительно более высокий риск развития инсульта (особенно геморрагического инсульта) среди пациентов, получавших ГР в детстве [28]. В противоположность этому последующее наблюдение 2543 пациентов с изолированной соматотропной недостаточностью, идиопатической низкорослостью или низким гестационным возрастом из других европейских стран не выявили никакого эффекта воздействия ГР и/или дозы на смертность или частоту развития сердечно-сосудистых событий [29].
Применение дозы препаратов ГР более 50 мкг/кг/день не рекомендовано. Полученные из той же базы данные в недавнем исследовании показали значительно более высокий риск развития инсульта (особенно геморрагического инсульта) среди пациентов, получавших ГР в детстве [28]. В противоположность этому последующее наблюдение 2543 пациентов с изолированной соматотропной недостаточностью, идиопатической низкорослостью или низким гестационным возрастом из других европейских стран не выявили никакого эффекта воздействия ГР и/или дозы на смертность или частоту развития сердечно-сосудистых событий [29].
Таким образом, имеющиеся данные относительно безопасности терапии ГР для детей с различными формами низкорослости определяют необходимость формирования персонализированного алгоритма диспансерного наблюдения пациента и должны включать информирование родителей ребенка об имеющихся сегодня сведениях о нежелательных явлениях как во время лечения, так и в отдаленные периоды жизни.
Применение высоких доз препаратов гормона роста при синдромальных формах низкорослости должно иметь взвешенный подход к сопоставлению показателей эффективности и безопасности лечения. Увеличение дозы ГР определяет рост шансов, отдаленных метаболических или злокачественных рисков, не обнаруженных в ходе проведенных на сегодняшний день исследований. Изменение характеристик пациентов, этнических особенностей и рост уровня ожирения в детстве может увеличить риск развития СД 2-го типа у получающих ГР.
Увеличение дозы ГР определяет рост шансов, отдаленных метаболических или злокачественных рисков, не обнаруженных в ходе проведенных на сегодняшний день исследований. Изменение характеристик пациентов, этнических особенностей и рост уровня ожирения в детстве может увеличить риск развития СД 2-го типа у получающих ГР.
Определенные побочные эффекты препаратов ГР, связанные с ускоренным ростом (прогрессирование сколиоза и эпифизеолиз) и другими неизвестными механизмами (внутричерепная гипертензия), встречаются редко, однако требуют упреждающего разъяснения и тщательного контроля.
Кроме того, следует помнить об отдаленных последствиях гормонального лечения. Поскольку исследования населения, не получающего ГР, свидетельствуют о том, что высокие нормальные уровни свободного ИФР-1 (часто выявляемые у детей, получавших ГР) могут увеличить риски онкологических заболеваний, потенциальные связи между воздействием ГР и будущими рисками возникновения неоплазии требуют постоянного контроля. И, наконец, соответствующий уровень допустимого риска для новейшей и потенциально самой большой группы пациентов, получавших ГР, — практически здоровых, но низкорослых детей — еще предстоит определить [30].
И, наконец, соответствующий уровень допустимого риска для новейшей и потенциально самой большой группы пациентов, получавших ГР, — практически здоровых, но низкорослых детей — еще предстоит определить [30].
Литературы
- Петеркова В. А. Гипофизарная карликовость: диагностика и лечение // Педиатрия. 2009. № 87 (02). С. 104–110.
- Ranke M. B., Lindberg A., Price D. A. et al. KIGS International Board. Age at growth hormone therapy start and first-year responsiveness to growth hormone are major determinants of height outcome in idiopathic short stature // Horm Res. 2007. № 68 (2). Р. 53–62.
- Kelnar C. J. Growth hormone for short children — whom should we be treating and why? // J R Coll Physicians Edinb. 2012. № 42 (1). Р. 32–33.
- Ranke M. B., Lindberg A. KIGS International Board. Observed and predicted growth responses in prepubertal children with growth disorders: guidance of growth hormone treatment by empirical variables // J Clin Endocrinol Metab.
 2010. № 95 (3). Р. 1229–1237.
2010. № 95 (3). Р. 1229–1237. - Cardoso D. F., Martinelli C. E. Jr, Campos V. C. et al. Comparison between the growth response to growth hormone (GH) therapy in children with partial GH insensitivity or mild GH deficiency // Arq Bras Endocrinol Metabol. 2014. № 58 (1). Р. 23–29.
- Hilczer M., Smyczynska J., Lewinski A. Parentally-adjusted deficit of height as a prognostic factor of the effectiveness of growth hormone (GH) therapy in children with GH deficiency // Neuro Endocrinol Lett. 2006. № 27 (1–2). Р. 149–152.
- Reiter E. O., Price D. A., Wilton P. et al. Effect of growth hormone (GH) treatment on the near-final height of 1258 patients with idiopathic GH deficiency: analysis of a large international database // J Clin Endocrinol Metab. 2006. № 91 (6). Р. 2047–2054.
- Colmenares A., González L., Gunczler P., Lanes R. Is the growth outcome of children with idiopathic short stature and isolated growth hormone deficiency following treatment with growth hormone and a luteinizing hormone-releasing hormone agonist superior to that obtained by GH alone? // J Pediatr Endocrinol Metab.
 2012. № 25 (7–8). Р. 651–657.
2012. № 25 (7–8). Р. 651–657. - Darendeliler F., Lindberg A., Wilton P. Response to growth hormone treatment in isolated growth hormone deficiency versus multiple pituitary hormone deficiency // Horm Res Paediatr. 2011. № 76. Suppl 1. Р. 42–46.
- Stevens A., Clayton P., Tatò L. et al. Pharmacogenomics of insulin-like growth factor-I generation during GH treatment in children with GH deficiency or Turner syndrome // Pharmacogenomics J. 2014. № 14 (1). Р. 54–62.
- Braz A. F., Costalonga E. F., Trarbach E. B. Genetic predictors of long-term response to growth hormone (GH) therapy in children with GH deficiency and Turner syndrome: the influence of a SOCS2 polymorphism // J Clin Endocrinol Metab. 2014. № 99 (9). Р. 1808–1813.
- Wilson T. A., Rose S. R., Cohen P. et al. Update of guidelines for the use of growth hormone in children: The Lawson Wilkins Pediatric Endocrinology Society Drug and Therapeutics Committee // J Pediatr.
 2003. № 143. Р. 415–421.
2003. № 143. Р. 415–421. - Bell J., Parker K. L., Swinford R. D. et al. Long-term safety of recombinant human growth hormone in children // J Clin Endocrinol Metab. 2010. № 95. Р. 167–177.
- Darendeliler F., Karagiannis G., Wilton P. Headache, idiopathic intracranial hypertension and slipped capital femoral epiphysis during growth hormone treatment: a safety update from the KIGS database // Horm Res. 2007. № 68. Suppl 5. P. 41–47.
- Grimberg А., DiVall S., Polychronakos C. et al. Guidelines for Growth Hormone and Insulin-Like Growth Factor-I Treatment in Children and Adolescents: Growth Hormone Deficiency, Idiopathic Short Stature, and Primary Insulin-Like Growth Factor-I Deficiency // Horm Res Paediatr. 2016. № 86. Р. 361–397.
- Mostoufi-Moab S., Isaacoff E. J., Spiegel D. et al. Childhood cancer survivors exposed to total body irradiation are at significant risk for slipped capital femoral epiphysis during recombinant growth hormone therapy // Pediatr Blood Cancer.
 2013. № 60. Р. 1766–1771.
2013. № 60. Р. 1766–1771. - Kim J. Y., Rosenfeld S. R., Keyak J. H. Increased prevalence of scoliosis in Turner syndrome // J Pediatr Orthop. 2001. № 21. Р. 765–766.
- Cohen P., Bright G. M., Rogol A. D. et al. Effects of dose and gender on the growth and growth factor response to GH in GH-deficient children: implications for efficacy and safety // J Clin Endocrinol Metab. 2002. № 87. Р. 90–98.
- Bareille P., Azcona C., Matthews D. R. et al. Lipid profile, glucose tolerance and insulin sensitivity after more than four years of growth hormone therapy in non-growth hormone deficient adolescents // Clin Endocrinol (Oxf). 1999. № 51. Р. 347–353.
- Aguiar-Oliveira M., Oliveira F. T., Pereira R. M. et al. Longevity in untreated congenital growth hormone deficiency due to a homozygous mutation in the GHRH receptor gene // J Clin Endocrinol Metab. 2010. № 95. Р. 714–721.
- Orme S. M., McNally R.
 J. Q., Cartwright R. A., Belchetz P. E. For the United Kingdom Acromegaly Study Group: Mortality and cancer incidence in acromegaly: a retrospective cohort study // J Clin Endocrinol Metab. 1998. № 83. Р. 2730–2734.
J. Q., Cartwright R. A., Belchetz P. E. For the United Kingdom Acromegaly Study Group: Mortality and cancer incidence in acromegaly: a retrospective cohort study // J Clin Endocrinol Metab. 1998. № 83. Р. 2730–2734. - Speakman J. R., Mitchell S. E. Caloric restriction // Mol Aspects Med. 2011. № 32. Р. 159–221.
- Cohen P., Clemmons D. R., Rosenfeld R. G. Does the GH-IGF axis play a role in cancer pathogenesis? // Growth Horm IGF Res. 2000. № 10. Р. 297–305.
- Wilton P., Mattsson A. F., Darendeliler F. Growth hormone treatment in children is not associated with an increase in the incidence of cancer: experience from KIGS (Pfizer International Growth Database) // J Pediatr. 2010. № 157. Р. 265–270.
- Mackenzie S., Craven T., Gattamaneni H. R. et al. Longterm safety of growth hormone replacement after CNS irradiation // J Clin Endocrinol Metab. 2011. № 96. Р. 2756–2761.
- Raman S.
 , Grimberg A., Waguespack S. G. et al. Risk of neoplasia in pediatric patients receiving growth hormone therapy — a report from the Pediatric Endocrine Society Drug and Therapeutics Committee // J Clin Endocrinol Metab. 2015. № 100. Р. 2192–2203.
, Grimberg A., Waguespack S. G. et al. Risk of neoplasia in pediatric patients receiving growth hormone therapy — a report from the Pediatric Endocrine Society Drug and Therapeutics Committee // J Clin Endocrinol Metab. 2015. № 100. Р. 2192–2203. - Carel J. C., Ecosse E., Landier F. et al. Long-term mortality after recombinant growth hormone treatment for isolated growth hormone deficiency or childhood short stature: preliminary report of the French SAGhE study // J Clin Endocrinol Metab. 2012. № 97. Р. 416–425.
- Poidvin A., Touze E., Ecosse E. et al. Growth hormone treatment for childhood short stature and risk of stroke in early adulthood // Neurology. 2014. № 83. Р. 780–786.
- Savendahl L., Maes M., Albertsson-Wikland K. et al. Long-term mortality and causes of death in isolated GHD, ISS, and SGA patients treated with recombinant growth hormone during childhood in Belgium, The Netherlands, and Sweden: preliminary report of 3 countries participating in the EU SAGhE study // J Clin Endocrinol Metab.
 2012. № 97. Р. 213–217.
2012. № 97. Р. 213–217. - Allen D. B. Growth hormone therapy for short stature: is the benefit worth the burden? // Pediatrics. 2006. № 118. Р. 343–348.
Е. Б. Башнина, доктор медицинских наук, профессор
О. С. Берсенева1
ФГБОУ ВО СЗГМУ им. И. И. Мечникова МЗ РФ, Санкт-Петербург
1 Контактная информация: [email protected]
Активное вещество СОМАТРОПИН (SOMATROPINUM) | Компендиум — справочник лекарственных препаратов
- Фармакологические свойства
- Показания СОМАТРОПИН
- Применение СОМАТРОПИН
- Противопоказания
- Побочные эффекты
- Особые указания
- Взаимодействия
- Передозировка
- Диагнозы
- Рекомендуемые аналоги
- Торговые наименования
Лекарственные препараты содержащие активное вещество СОМАТРОПИН
Генотропин
порошок лиофилизированный для раствора для инъекций 16 МЕ (5,3 мг) предварительно заполненная ручка с растворителем, № 1
Pfizer Inc.
Цены в аптеках
Генотропин
порошок лиофилизированный для раствора для инъекций 36 МЕ/мл предварительно заполненная ручка с растворителем, № 1
Pfizer Inc.
Цены в аптеках
Зомактон
порошок для приготовления инъекционного раствора 4 мг флакон + растворитель в ампулах по 3,5 мл, № 1
Ferring GmbH
Цены в аптеках
Соматин
лиофилизат для раствора для инъекций 1,3 мг флакон с растворителем в ампулах по 1 мл, № 1
Биофарма ФЗ
Цены в аптеках
Соматин
лиофилизат для раствора для инъекций 1,3 мг флакон с растворителем во флаконах по 1 мл, № 1
Биофарма ФЗ
Цены в аптеках
рекомбинантный гормон роста человека. Представляет собой пептид из 191 аминокислоты, идентичный человеческому гипофизарному гормону роста по аминокислотной последовательности и составу, а также по пептидной карте, изоэлектрической точке, молекулярной массе, изомерной структуре и биологической активности.
Оказывает анаболическое и антикатаболическое действие, влияет на метаболизм, рост и развитие тела. Взаимодействует со специфическими рецепторами клеток разных типов, включая миоциты, гепатоциты, адипоциты, лимфоциты и гемопоэтические клетки. Некоторые его эффекты опосредованы другим классом гормонов — соматомединами (IGF1 и IGF2).
Взаимодействует со специфическими рецепторами клеток разных типов, включая миоциты, гепатоциты, адипоциты, лимфоциты и гемопоэтические клетки. Некоторые его эффекты опосредованы другим классом гормонов — соматомединами (IGF1 и IGF2).
В зависимости от дозы соматропин вызывает повышение уровня IGF1, IGFBP3, неэстерифицированных жирных кислот и глицерина, снижение уровня мочевины в крови и азота в моче, снижение экскреции натрия и калия. При применении в высоких дозах возможно относительное насыщение эффектов соматропина. Это не относится к гликемии и экскреции с мочой С-пептида, которые значительно повышаются лишь после применения в высоких дозах (20 мг).
Фармакокинетика имеет линейный характер при применении в дозах до 8 МЕ (2,67 мг). В более высоких дозах (60 МЕ, или 20 мг) нельзя исключить некоторую степень нелинейности, которая тем не менее не имеет клинического значения. После в/в введения здоровым добровольцам объем распределения в равновесном состоянии составляет почти 7 л, общий клиренс — 15 л/ч, тогда как почечный клиренс незначительный. T½ — 20–35 мин.
T½ — 20–35 мин.
После однократного п/к и в/м введения терминальный T½ несколько больше — 2–4 ч. Концентрация гормона роста в крови достигает максимума приблизительно через 4 ч и возвращается к исходному уровню в течение 24 ч, что свидетельствует об отсутствии кумуляции гормона роста при повторных введениях. Биодоступность при обоих путях введения составляет 70–90%.
задержка роста у детей, обусловленная снижением или отсутствием секреции эндогенного гормона роста; задержка роста у девочек с дисгенезией гонад (синдром Тернера), подтвержденная данными хромосомного анализа.
дозу следует устанавливать индивидуально в зависимости от площади поверхности или массы тела больного.
Вводить рекомендуется перед сном согласно следующим рекомендациям:
Задержка роста вследствие неадекватной секреции эндогенного гормона роста: 0,7–1,0 мг/м2 или 0,026–0,035 мг/кг/сут п/к.
Задержка роста у девочек вследствие дисгенезии гонад (синдром Тернера): 1,4 мг/м2/сут или 0,045–0,050 мг/кг п/к.
Сопутствующая терапия неандрогенными анаболическими стероидами у больных с синдромом Тернера может повысить скорость роста.
Лечение прекращают при достаточном для взрослого человека увеличении роста или в случае закрытия эпифизов.
нельзя назначать детям при закрытии эпифизов (прекращение роста костей), а также больным с повышенной чувствительностью к соматропину, при наличии новообразований.
примерно в 10% случаев отмечаются гиперемия и зуд кожи в месте инъекции.
У некоторых больных могут образовываться антитела к соматропину; клиническое значение этого факта не установлено. В единичных случаях, если невысокий рост обусловлен делецией в генном комплексе гормона роста, лечение гормоном роста может вызвать продукцию антител, тормозящих процесс роста.
Может иметь место эпифизиолиз с поражением бедренного сустава. Ребенок с хромотой невыясненного генеза должен быть обследован.
клинический опыт применения гормона роста в период беременности ограничен. В ходе экспериментальных исследований не установлено прямого или опосредованного негативного влияния на течение беременности, развитие плода, на роды и постнатальное развитие, однако при назначении в период беременности следует соблюдать осторожность.
В ходе экспериментальных исследований не установлено прямого или опосредованного негативного влияния на течение беременности, развитие плода, на роды и постнатальное развитие, однако при назначении в период беременности следует соблюдать осторожность.
Эндогенные белковые гормоны могут экскретироваться с грудным молоком, однако вероятность абсорбции неизмененного белка из пищеварительного тракта ребенка грудного возраста низкая.
Лечение следует проводить под систематическим наблюдением специалиста, который имеет опыт диагностики и лечения больных с недостаточностью гормона роста.
Во время терапии соматропином может развиться гипотиреоз, поэтому необходимо периодически проводить исследование функции щитовидной железы. Для получения достаточного терапевтического эффекта в процессе лечения гормоном роста возможный гипотиреоз следует корригировать назначением тиреоидных гормонов.
Больные с внутри- или внечерепными новообразованиями в стадии ремиссии, которые получают терапию гормоном роста, должны проходить врачебное обследование через определенные промежутки времени. Больные с нарушением роста, обусловленным внутричерепной опухолью, должны периодически проходить обследование по поводу прогрессирования или рецидивов основного заболевания.
Больные с нарушением роста, обусловленным внутричерепной опухолью, должны периодически проходить обследование по поводу прогрессирования или рецидивов основного заболевания.
Сообщалось о более частых случаях лейкоза у детей с недостаточностью гормона роста, которые не лечились или лечились гормоном роста, по сравнению с детьми, у которых не отмечен дефицит гормона роста. Причинной связи с терапией гормоном роста не установлено.
В случае развития интенсивной головной боли, нарушений зрения, тошноты и рвоты рекомендовано обследование глазного дна для выявления отека диска зрительного нерва. В случае подтверждения диагноза следует учитывать возможность развития доброкачественной внутричерепной гипертензии, в связи с чем лечение соматропином необходимо прекратить. Если лечение гормоном роста впоследствии возобновляют, требуется тщательный мониторинг симптомов внутричерепной гипертензии, в случае ее рецидива лечение следует прекратить.
Введение гормона роста сопровождается кратковременной фазой гипогликемии в течение 2 ч, а потом в течение следующих 2–4 ч — повышением уровня глюкозы в крови, несмотря на высокую концентрацию инсулина.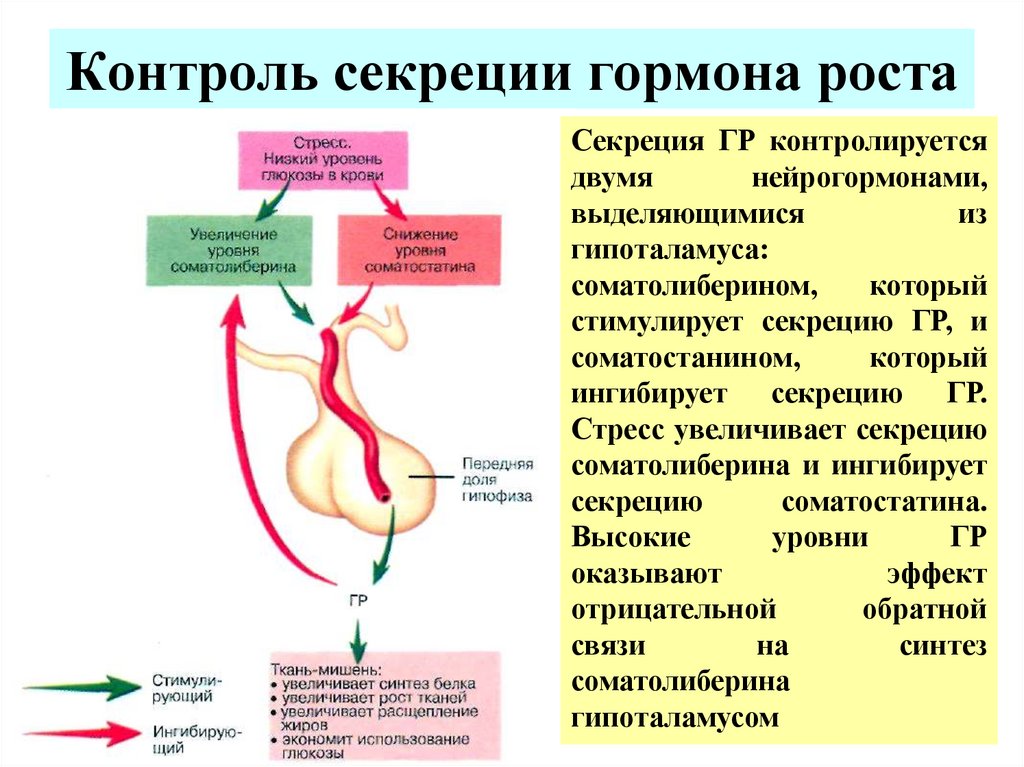 Для выявления резистентности к инсулину больному следует провести тест на толерантность к глюкозе.
Для выявления резистентности к инсулину больному следует провести тест на толерантность к глюкозе.
У больных сахарным диабетом или в случае наличия сахарного диабета в семейном анамнезе соматропин применяют с осторожностью. У больных сахарным диабетом может потребоваться коррекция антидиабетической терапии.
У всех пациентов с острыми тяжелыми заболеваниями необходимо оценить соотношение между возможным терапевтическим эффектом от применения гормона роста и потенциальным риском.
Чтобы предотвратить развитие липоатрофии, необходимо изменять места инъекций. В случае продолжительного отека или тяжелой парестезии необходимо снизить дозу соматропина, чтобы предотвратить развитие кистевого туннельного синдрома.
одновременная терапия ГКС может замедлять терапевтический эффект соматропина. Может повышать клиренс соединений, метаболизируемых цитохромом Р450 3А4 (половые гормоны, кортикостероиды, противосудорожные средства и циклоспорин).
вероятно развитие гипогликемии с последующей гипергликемией. Хроническая передозировка может стать причиной развития гигантизма и (или) акромегалии, которые сочетаются с другими известными проявлениями избытка гормона роста у человека.
Хроническая передозировка может стать причиной развития гигантизма и (или) акромегалии, которые сочетаются с другими известными проявлениями избытка гормона роста у человека.
Инъекции гормона роста: применение и побочные эффекты
Гормоны играют роль почти во всех основных функциях организма, включая рост. Если организм не вырабатывает достаточно, человеку могут потребоваться инъекции гормона роста.
Несколько желез в организме вырабатывают гормоны, но эксперты в области здравоохранения считают гипофиз главной управляющей железой. Он не только контролирует другие железы, но и вырабатывает гормон, запускающий рост.
Гипофиз находится в головном мозге ниже гипоталамуса. Он выделяет гормоны в ответ на химические сигналы гипоталамуса.
Гормон роста человека (HGH) помогает влиять на рост, а также на формирование костей и мышц тела. Это имеет решающее значение для процессов, связанных с нормальным ростом и развитием человека.
Генетические факторы могут привести к недостатку гормона роста у детей. Повреждение гипофиза является частой причиной дефицита у взрослых.
Повреждение гипофиза является частой причиной дефицита у взрослых.
В этой статье мы рассмотрим причины использования гормона роста, функцию гормонов роста и возможные побочные эффекты.
Поделиться на PinterestЛекарство от гормона роста может помочь детям и взрослым с дефицитом гормона роста.
Гормон роста необходим для роста, особенно у детей, но он также участвует во многих других процессах в организме, включая плотность костей, мышечную массу и настроение.
Различные гормоны контролируют различные функции и процессы организма, включая рост и развитие, обмен веществ, половую функцию и размножение, а также настроение.
Помогает перерабатывать белок и ускоряет расщепление жира, обеспечивая энергию, необходимую для роста тканей.
Уровень гормона роста может меняться в течение дня, и определенную роль играет физическая активность.
Упражнения и подобные действия могут привести к естественному повышению уровня. Сон, стресс и низкий уровень сахара в крови также повышают уровень гормона роста.
Даже небольшие изменения уровня гормона роста влияют на организм.
Слишком мало или слишком много гормона роста может вызвать серьезные проблемы роста. Слишком низкий уровень гормона роста является одной из основных причин низкого роста и таких состояний, как карликовость.
Некоторые люди используют гормон роста, потому что считают, что он нарастит мышечную массу, улучшит работоспособность или замедлит старение. Однако существующие данные не поддерживают использование гормона роста для этих целей.
Дети с низким уровнем дефицита гормона роста могут быть или не быть меньше при рождении. Проблемы с ростом могут появиться со временем, например, если они меньше своих одноклассников и растут менее чем на 2 дюйма в год.
У некоторых детей гормон роста не вырабатывается при рождении, и его уровень остается низким на протяжении всей жизни.
Симптомы дефицита гормона роста у детей:
- выглядят намного моложе, чем другие дети их возраста
- пухлое телосложение
- нарушение роста волос
- задержка полового созревания
- низкий рост
У некоторых детей недостаток гормона роста является частью генетического заболевания, но иногда причина дефицита неизвестна.
У взрослых недостаток гормона роста часто возникает из-за повреждения гипофиза, которое может быть необратимым. Повреждение могло произойти в детстве или во взрослом возрасте.
Другие причины включают:
- лучевая терапия
- травма головы
- инфекции, такие как менингит
Проблемы в гипофизе с выработкой гормона роста обычно возникают из-за опухоли гипофиза.
Гипофиз может быть поврежден самой опухолью или в результате лечения, такого как хирургическое вмешательство и лучевая терапия.
У взрослых недостаток гормона роста может вызвать ряд различных проблем, в том числе:
- тревогу и депрессию
- увеличение жира вокруг талии
- повышенный риск сердечных заболеваний и инсульта
- слабое сердце
- слабые мышцы и кости
- усталость
- сниженная способность мыслить
- другие состояния
Дефицит гормона роста также может быть комбинацией дефицита одного или нескольких гормонов.
При некоторых заболеваниях также может быть полезно лечение гормоном роста.
К ним относятся:
- Синдром Тернера: Женщины с этим заболеванием обычно имеют недоразвитые женские половые признаки.
- Синдром Прадера-Вилли: Генетическое заболевание вызывает слабый мышечный тонус, трудности с кормлением, плохой рост и задержку развития.
- Синдром Нунан: Это генетическое заболевание препятствует правильному развитию различных частей тела.
- Хроническая болезнь почек
Поделиться на PinterestЧеловек может делать инъекции гормона роста дома или получать гормон в кабинете врача.
Наиболее распространенным методом лечения как взрослых, так и детей является терапия гормоном роста с использованием разработанных в лаборатории инъекций гормона роста.
Дозы вводят несколько раз в неделю или ежедневно, в зависимости от того, насколько серьезен дефицит. Производители разработали гормон роста, чтобы имитировать поведение естественного гормона роста в организме. Его назначит врач.
Его назначит врач.
Лечение гормоном роста можно проводить самостоятельно или назначать врачом. Лечение часто назначают на несколько лет. Пациенты будут посещать своего врача каждый месяц или около того, чтобы проверить свое состояние.
Будут проведены анализы крови, чтобы определить, нужен ли дополнительный гормон роста и следует ли увеличить, уменьшить или прекратить лечение. Уровень холестерина, уровень сахара в крови и плотность костей также будут проверены, чтобы убедиться, что они здоровы.
Прием гормона роста может повлиять на реакцию организма на инсулин, который контролирует уровень сахара в крови. Дефицит гормона роста также может привести к высокому уровню холестерина и ломкости костей, если его не лечить.
Конкретное лечение дефицита гормона роста зависит от человека.
Врачи основывают это лечение на определенных факторах, таких как:
- возраст
- общее состояние здоровья и история болезни
- степень заболевания
- переносимость специфического лечения
- ожидания от лечения
- по выбору пациента
Чем раньше будет проведено лечение дефицита гормона роста у детей, тем больше шансов, что они вырастут почти до нормального взрослого роста.
В течение первых 3 лет лечения дети могут прибавить в росте до 4 дюймов и более. Еще 3 дюйма или более могут вырасти в течение следующих 2 лет.
Многим взрослым приходится принимать гормон роста до конца своей жизни.
Каждый, кто принимает гормон роста, должен проходить регулярный контроль для оценки безопасности и эффективности гормона.
Целью лечения гормоном роста у взрослых и детей является восстановление энергии, обмена веществ и улучшение развития или формы тела. Это может помочь уменьшить общее количество жира в организме, особенно вокруг живота.
Инъекции гормона роста также могут помочь улучшить силу и толерантность к физическим нагрузкам, а также снизить риск сердечных заболеваний у тех, у кого не хватает гормона роста.
У многих людей улучшается общее качество жизни.
Большинство людей хорошо переносят инъекции гормона роста с небольшими проблемами.
Тем не менее, возможные побочные эффекты включают:
- боли в мышцах
- дискомфорт в суставах
- головные боли
- отек рук и ног
Те, у кого есть эти симптомы или другие проблемы, должны обратиться к своему врачу. При необходимости они могут изменить дозу, чтобы облегчить симптомы.
При необходимости они могут изменить дозу, чтобы облегчить симптомы.
Инъекции гормона роста не рекомендуются людям, у которых есть:
- опухоли
- рак
- серьезные заболевания
- серьезные проблемы с дыханием
- множественные травмы
- осложнения после операции на открытом сердце или брюшной полости
Гормон роста может повлиять на использование инсулина в организме, поэтому люди с диабетом должны тщательно контролировать уровень сахара в крови.
В зависимости от причины дефицита гормона роста могут потребоваться другие виды лечения.
Для лечения опухоли гипофиза может потребоваться хирургическое вмешательство или облучение. Гормоны гипофиза, возможно, также придется принимать, чтобы исправить работу железы, которая не работает должным образом.
Слишком много человеческого гормона роста
Если уровни гормона роста слишком высоки у взрослых, они могут испытывать:
- боль в мышцах или суставах
- задержку жидкости, приводящую к отеку
- синдром запястного канала
Долгосрочное использование инъекций гормона роста может вызвать состояние, называемое акромегалией.
Взрослые не могут стать выше при использовании синтетического гормона роста. Высокие дозы утолщают кости человека, а не удлиняют их.
У людей с акромегалией наблюдается разрастание костей, особенно в руках, ногах и лице.
Область кожи также может быть поражена и может стать толстой, грубой и покрытой волосами. Избыточные уровни гормона роста также могут привести к высокому кровяному давлению и сердечным заболеваниям.
Поделиться на PinterestСпортсмены иногда используют гормон роста для наращивания мышечной массы и повышения производительности, но это не является законным в соревновательных видах спорта в США.
Инъекции гормона роста также стали популярными для немедицинского использования. Бодибилдеры и спортсмены иногда используют их, чтобы получить большие мышцы, больше энергии и повышенную выносливость.
Они считаются препаратами, повышающими работоспособность, и запрещены в профессиональном спорте.
Инъекции гормона роста также рекламируются как средство против старения или для снижения веса.
Многие люди стремятся увеличить свою энергию, а также бороться с уменьшением мышечной и костной массы, которое происходит с возрастом.
Эндокринное общество не рекомендует инъекции гормона роста взрослым или детям, если у них нет дефицита гормона роста.
Недостаточно доказательств того, что инъекции гормона роста могут замедлить процесс старения, и исследования показывают, что он не улучшает спортивные результаты. Часто возникают побочные эффекты, особенно задержка жидкости.
Использование их по любой немедицинской причине является незаконным в Соединенных Штатах.
Инъекции гормона роста предназначены для взрослых или детей с недостатком гормона роста и должны назначаться только врачом.
Дети и взрослые с низким уровнем гормона роста должны обеспечить достаточное количество сна, сбалансированную диету, регулярные физические упражнения и следовать рекомендациям врача.
Q:
Кажется, люди заинтересованы в использовании гормона роста, чтобы иметь более спортивное тело, лучше заниматься спортом и предотвращать старение. Это хорошая идея?
Это хорошая идея?
A:
Гормон роста является сильнодействующим лекарством, которое может вызывать серьезные побочные эффекты. Поэтому человеку необходимо взвесить преимущества и риски. Перевешивают ли потенциальные выгоды риски?
Для тех, у кого нет дефицита гормона роста, ответ — нет. Очень мало данных подтверждают идею о том, что гормон роста помогает людям с нормальным уровнем гормона роста.
Он может улучшить мышечную массу у спортсменов и пожилых людей, но, по-видимому, не увеличивает силу или производительность.
Он также не улучшает факторы риска хронических заболеваний, таких как диабет или сердечные заболевания. Нет надежных доказательств того, что он может предотвратить старение.
Karen Gill, MD
Ответы представляют мнения наших медицинских экспертов. Весь контент носит исключительно информационный характер и не должен рассматриваться как медицинский совет.
Было ли это полезно?
Побочные эффекты у мужчин и женщин
Обзор
Гормон роста человека (hGH) представляет собой естественный гормон, вырабатываемый гипофизом. Это важно для роста, регенерации и размножения клеток.
Это важно для роста, регенерации и размножения клеток.
Гормон роста помогает поддерживать, строить и восстанавливать здоровые ткани головного мозга и других органов. Этот гормон может помочь ускорить заживление после травмы и восстановить мышечную ткань после тренировки. Это помогает нарастить мышечную массу, повысить метаболизм и сжечь жир.
Гормон роста также улучшает качество и внешний вид кожи. Говорят, что он замедляет процесс старения и лечит возрастные заболевания. Однако исследования, подтверждающие эти утверждения, ограничены.
Гормон роста стимулирует метаболические процессы в клетках, чтобы активировать обмен веществ. Он стимулирует печень вырабатывать инсулиноподобный белок, который производит хрящевые клетки. Это играет роль в росте костей и органов, а также в синтезе мышечного белка.
Хотя hGH является природным веществом, он также доступен в синтетических формах в качестве лечения или добавки. Но каковы риски его принятия?
Синтетический гормон роста используется для лечения задержки роста у детей и взрослых. Его также можно использовать для лечения взрослых с синдромом короткой кишки или потерей мышечной массы из-за ВИЧ или СПИДа.
Его также можно использовать для лечения взрослых с синдромом короткой кишки или потерей мышечной массы из-за ВИЧ или СПИДа.
Отсутствие роста может быть результатом медицинских причин, таких как:
- хроническая болезнь почек
- дети, родившиеся с низкой массой тела при рождении
- синдром Прадера-Вилли
- дефицит или недостаточность чГР к опухолям гипофиза или родственному лечению
- болезнь атрофии мышц
Инъекции чГР могут помочь людям с дефицитом гормона роста:
- повысить физическую работоспособность
- улучшить плотность костей многие люди используют гормон роста для повышения своих спортивных способностей. Иногда его используют в сочетании с анаболическими стероидами для увеличения мышечной массы и улучшения спортивных результатов.
Некоторые люди считают, что гормон роста обладает омолаживающим эффектом, поскольку естественный уровень гормона роста с возрастом снижается. Также говорят, что он естественным образом увеличивает уровень тестостерона.
 Однако следует отметить, что не все эти преимущества были научно доказаны. Использование гормона роста в спортивных и омолаживающих целях вызывает споры из-за отсутствия научных доказательств и его потенциальных побочных эффектов.
Однако следует отметить, что не все эти преимущества были научно доказаны. Использование гормона роста в спортивных и омолаживающих целях вызывает споры из-за отсутствия научных доказательств и его потенциальных побочных эффектов.Гормон роста вводят внутримышечно (в/м) и подкожно (под кожу), если он назначен. Иногда нелегальные производители также предлагают hGH в инъекционной форме.
Гормон роста и вещества, стимулирующие выработку гормона роста, продаются некоторыми компаниями через Интернет в виде пищевых добавок, которые утверждают, что обладают теми же преимуществами, что и инъекции. Эти добавки иногда называют релизерами гормона роста человека. Говорят, что некоторые из них повышают уровень гормона роста в организме из-за таких ингредиентов, как аминокислоты.
Тем не менее, нет никаких доказательств того, что эти добавки дают те же результаты, что и прописанный чГР. Существуют также гомеопатические препараты, содержащие человеческий гормон роста. Доказательств, подтверждающих их преимущества, не хватает.

SeroVital — популярная марка пищевых добавок. Говорят, что он способен естественным образом повышать уровень гормона роста из-за содержащихся в нем аминокислот. Говорят, что это имеет антивозрастной эффект. SeroVital также утверждает, что укрепляет кости, увеличивает мышечную массу и уменьшает жировые отложения. Эти утверждения нуждаются в дополнительном изучении. SeroVital не содержит hGH.
Есть несколько побочных эффектов, которые могут сопровождать использование гормона роста. Эти побочные эффекты возможны с прописанной версией, а также с незаконной формой гормона роста, поскольку содержание не полностью известно и не регулируется. Побочные эффекты могут затронуть пожилых людей больше, чем молодых людей. Долгосрочные эффекты гормона роста неизвестны.
Возможные побочные эффекты избыточных инъекций гормона роста включают:
- синдром запястного канала
- боль в нервах, мышцах или суставах
- отек рук и ног из-за задержки жидкости (отек)
- высокий уровень холестерина
- онемение и покалывание кожи
- повышенный риск сердечно-сосудистых заболеваний и диабета
- рост раковых опухолей
- рост черт лица, рук и ног (акромегалия)
- изменения настроения, зависимость и синдром отмены
- увеличенное сердце
- низкий уровень сахара в крови
- повреждение печени
- усталость
- увеличение груди у мужчин (гинекомастия) содержат hGH.
 Побочные эффекты аминокислот в SeroVital могут включать:
Побочные эффекты аминокислот в SeroVital могут включать:- stomach pain
- nausea
- vomiting
- diarrhea
- constipation
- bloating
- increased asthma symptoms
- gout
- low blood pressure
- allergic reaction
- heartburn
HGH should be used with care and рассмотрение. Используйте только hGH, который вы получаете по рецепту врача. Регулярно проверяйтесь у своего врача, пока вы его принимаете.
Обратите особое внимание на то, как реагирует ваш организм, и если вы испытываете какие-либо побочные реакции. Если вы хотите укрепить свое тело или улучшить свое здоровье, но у вас нет заболеваний, вызывающих дефицит гормона роста, вы можете рассмотреть возможность поиска других способов сделать это. Соблюдайте здоровую диету, регулярно занимайтесь спортом и придерживайтесь здоровых привычек, чтобы улучшить общее состояние здоровья и самочувствие.
Q:
Может ли hGH дать женщинам массивные, мужественные мышцы?
Анонимный пациент
A:
Нет никаких доказательств того, что прием гормона роста вызывает у здоровых женщин (с нормальным уровнем гормона роста) появление объемных мышц.


 2010. № 95 (3). Р. 1229–1237.
2010. № 95 (3). Р. 1229–1237. 2012. № 25 (7–8). Р. 651–657.
2012. № 25 (7–8). Р. 651–657. 2003. № 143. Р. 415–421.
2003. № 143. Р. 415–421. 2013. № 60. Р. 1766–1771.
2013. № 60. Р. 1766–1771. J. Q., Cartwright R. A., Belchetz P. E. For the United Kingdom Acromegaly Study Group: Mortality and cancer incidence in acromegaly: a retrospective cohort study // J Clin Endocrinol Metab. 1998. № 83. Р. 2730–2734.
J. Q., Cartwright R. A., Belchetz P. E. For the United Kingdom Acromegaly Study Group: Mortality and cancer incidence in acromegaly: a retrospective cohort study // J Clin Endocrinol Metab. 1998. № 83. Р. 2730–2734. , Grimberg A., Waguespack S. G. et al. Risk of neoplasia in pediatric patients receiving growth hormone therapy — a report from the Pediatric Endocrine Society Drug and Therapeutics Committee // J Clin Endocrinol Metab. 2015. № 100. Р. 2192–2203.
, Grimberg A., Waguespack S. G. et al. Risk of neoplasia in pediatric patients receiving growth hormone therapy — a report from the Pediatric Endocrine Society Drug and Therapeutics Committee // J Clin Endocrinol Metab. 2015. № 100. Р. 2192–2203. 2012. № 97. Р. 213–217.
2012. № 97. Р. 213–217. Однако следует отметить, что не все эти преимущества были научно доказаны. Использование гормона роста в спортивных и омолаживающих целях вызывает споры из-за отсутствия научных доказательств и его потенциальных побочных эффектов.
Однако следует отметить, что не все эти преимущества были научно доказаны. Использование гормона роста в спортивных и омолаживающих целях вызывает споры из-за отсутствия научных доказательств и его потенциальных побочных эффектов.
 Побочные эффекты аминокислот в SeroVital могут включать:
Побочные эффекты аминокислот в SeroVital могут включать: