что это такое и какое лечение предстоит, а также о чем говорят повышенная эхогенность простаты, изоэхогенные и гиперэхогенные образования
В заключении ультразвукового обследования врач может сделать заключение о наличии диффузных изменений предстательной железы.
С такой формулировкой сталкиваются многие мужчины, но мало кто знает, как именно расшифровывается этот показатель, представляет ли он опасность и требует ли дальнейшего лечения.
Скрыть содержание
- Диффузные изменения предстательной железы: что это значит?
- Причины заболевания
- Классификация простаты
- Симптомы болезни
- Особенности диагностики
- Лечение недуга у мужчин
- Заключение
- Полезное видео
Диффузные изменения предстательной железы: что это значит?
Диффузные изменения простаты — показатель, который специалист может выявить во время проведении ультразвуковой диагностики простаты. Как правило, он указывает на наличие дистрофических повреждений органа в результате опухолевых образований, протекающего воспалительного процесса или абсцесса.
Это те самые отличительные признаки, которые могут указывать на наличие различных патологий и заболеваний как в остропротекающей, так и в хронической стадии.
Эти признаки помогают врачу правильно дифференцировать кисту или туберкулез простаты от раковой опухоли, простатит от аденомы и другие состояния, чтобы правильно установить диагноз.
Надеемся вышепредставленная информация помогла вам узнать определение диффузного изменения паренхимы предстательной железы, что это такое.
Причины заболевания
В настоящее время специалисты выделяют следующие причины изменений паренхимы простаты:
- Болезни передающиеся половым путем, вызванные уреаплазмозмами, микоплазмами, хламидиозом и другими микроорганизмами.
- Бактериальные инфекции, вызванные кишечными палочками, энтерококками, гонококками, бактериями туберкулеза и другими патогенными микроорганизмами.
В норме внешний вид железы должен быть симметричным, иметь правильную округлую форму с четкими контурами.
Должна прослеживаться визуализация семенных пузырьков, а диаметр составлять не более 25 мм. Но, так бывает не всегда.
При воздействии патогенных факторов ткани начинают изменяться. Это может происходить в результате разрастания и преобразования соединительной ткани, нарушений обмена веществ на клеточном уровне, уплотнения тканей в результате воспалительного процесса, опухолей, недостаточного кровообращения в тканях.
Классификация простаты
Диффузные изменения можно дифференцировать исходя из типа повреждения: атрофия, гипоплазия, гиперплазия, дисплазия. Рассмотрим подробнее каждое из состояний.
- Атрофические процессы в тканях — часто возникают в следствии гормональных возрастных изменений, в результате которых нарушается строение и функционирование половых органов, железа начинает отмирать. Атрофия может развиться так же из-за воспаления яичек (орхита).
- Гипоплазия — развивается довольно в молодом возрасте от 16 до 19 лет в результате недоразвития простаты.
Патологию не трудно распознать по анализу на гормоны и УЗИ.
- Гиперплазия стенок простаты — возникает на фоне длительно протекающего воспалительного процесса.
В результате эпителиальные клетки железы разрастаются и образуют характерные для гиперплазии узелки, сдавливающие мочевыводящий канал и нарушающие нормальный отток мочи.
В медицине гиперплазию называют аденомой (доброкачественное новообразование, не дающие метастаз).
- Диплазия — характеризуется разрастанием на стенках простаты участков ткани (атипичных клеток), нехарактерных для этого органа. Болезнь может протекать в трех стадиях: первая (легкая), вторая (средняя) и третья (выраженная). Последняя из них наиболее опасна, поскольку может переродиться в онкологию.
Симптомы болезни
Признаки диффузных изменений паренхимы предстательной железы будут различаться в зависимости от формы и вида заболеваний:
- Так, при простатите проявляются признаки воспалительного процесса: чувство жжения, дискомфорт при эякуляции, проблемы с мочеиспусканием, снижение полового влечения, учащенные позывы опорожнить мочевой пузырь.
На УЗИ будет заметно увеличение простаты, зональная эхогенность и тканевых уплотнения для хронической формы.
- При аденоме пациента беспокоят: чувство неполного опустошения мочевого пузыря, частые позывы к мочеиспусканию, трудности с отхождением мочи, слабый напор струи и другие. На УЗИ будет заметно увеличение размеров простаты и наличие аденоматозных узелковых образований.
Симптомы заболеваний простаты и их проявления индивидуальны и будут проявляться по разному у каждого пациента.
Особенности диагностики
Наличие диффузных изменений можно обнаружить во время проведения УЗИ. Врач фиксирует все признаки, замеченные на экране монитора и заносит их в заключение.
Записи специалиста могут говорить:
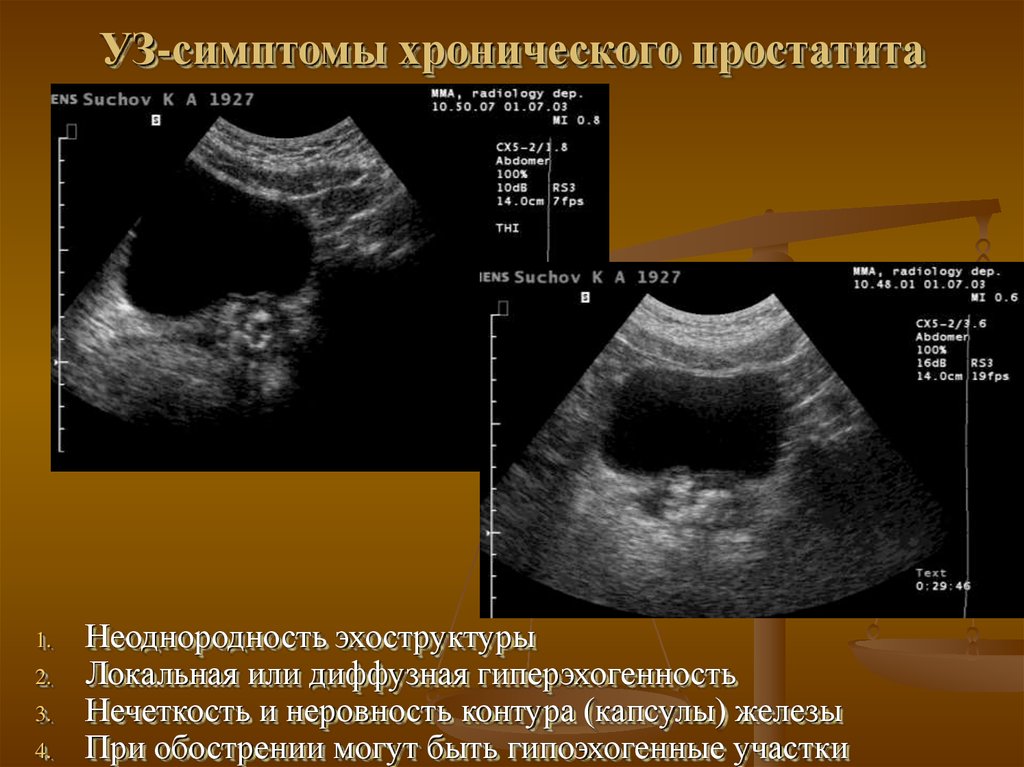
- Сниженная эхогенность частей простаты может прослеживаться при наличии хронического простатита. При этом воспаленные пораженные ткани уплотняются и в полной мере не просвечиваются на экране монитора.
- Анэхогенные зоны выявляются при абсцессе железы.
- Гиперэхогенные участки в предстательной железе могут указывать на простатит, протекающий в острой стадии. Часто сопровождается не только характерной симптоматикой, но и повышенной температурой тела.
- Если структура предстательной железы неоднородная, то это может быть связано с возникновением фиброза, кальцинатов, отёка, гноя и отмечаться при разных заболеваниях.
- Изоэхогенные образования в предстательной железе почти всегда означают, что в органе найдено опухолевое заболевание.
- Гипоэхогенное образование в предстательной железе может указывать на рак, периферически расположенный узел доброкачественной гиперплазии, а так же на простатическую интраэпителиальную опухоль.
- Повышенная эхогенность предстательной железы — что это такое? Если эхогенность предстательной железы повышена это может говорить о наличии аденомы, узловой формы аденомы, гиперплазии и злокачественных новообразований.
- Если эхоструктура неоднородная (предстательной железы), то это может указывать на развитие воспалительных процессов в предстательной железе.
Теперь, когда вы знаете о чем, говорят диффузные изменения паренхимы простаты, лечение заболевания — следующая тема, которую мы рассмотрим в данной статье.
Лечение недуга у мужчин
Назначение медикаментозных препаратов, схема лечения и продолжительность терапии будут исходить из вида заболевания, а так же тяжести и особенностей его протекания. Четкой схемы нет.
Она подбирается врачом в каждом конкретном случае и только после комплексного обследования пациента и постановки правильного диагноза. Поэтому настоятельно рекомендуем обратиться к специалисту за помощью и не заниматься самолечением.
Заключение
Помните, что выявление диффузных изменений всегда должно быть поводом для беспокойства. Этот признак в 99% случаев будет указывать на наличие какой-либо патологии.
Пациенту важно пройти комплексную диагностику, чтобы правильно определить развитие болезни.
Надеемся, статья помогла вам получше узнать о структурных диффузных изменениях предстательной железы, что это такое, и какие действия необходимо совершить для лечения недуга.
Полезное видео
Как проводится УЗИ простаты, рассказано на видео:
Наверх
Доброкачественная гиперплазия предстательной железы (ДГПЖ, аденома)
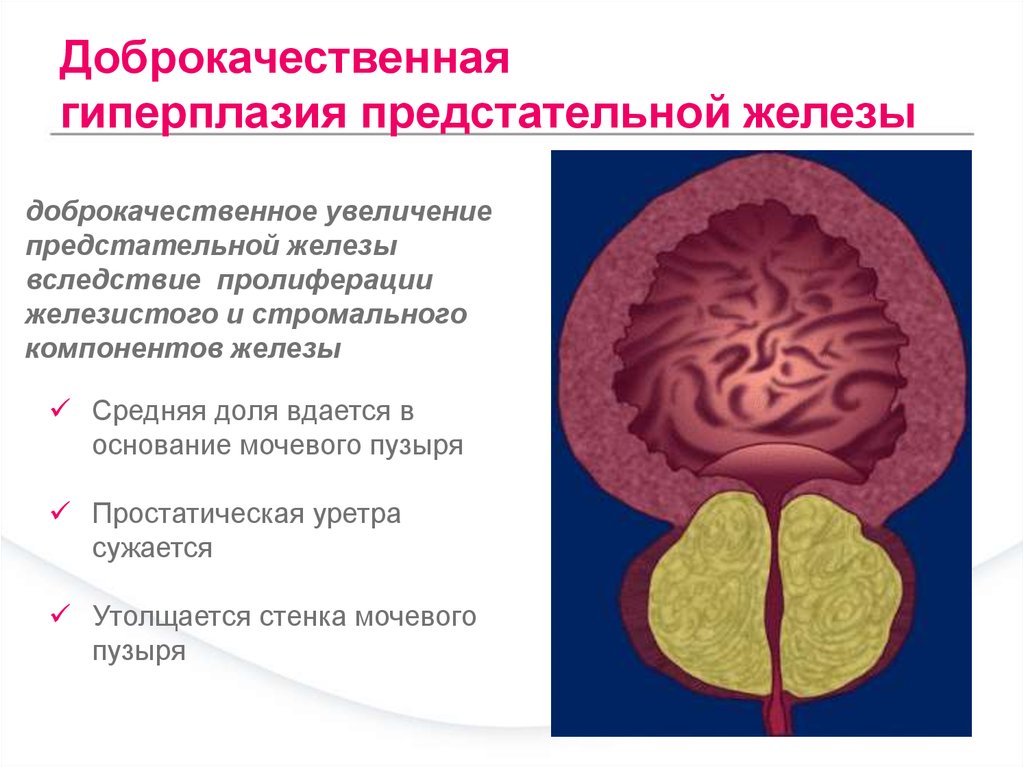
ДГПЖ (доброкачественная гиперплазия предстательной железы, аденома простаты) – это доброкачественное разрастание тканей железы, увеличение её в объёме. Разросшаяся железа сдавливает проходящий через неё мочеиспускательный канал, вызывая нарушения мочеиспускания – это основной симптом заболевания.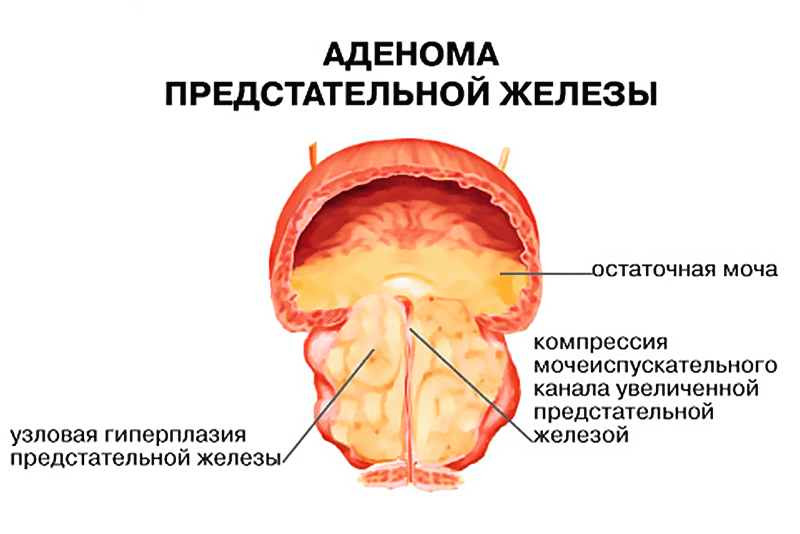
Доброкачественная гиперплазия предстательной железы выявляется у 20% мужчин 40 лет, 70% — 60 лет, 90% — 80 лет. Основной причиной развития ДГПЖ является изменение гормонального фона мужчины (снижение с возрастом уровня тестостерона).
Возможные осложнения ДГПЖ
- Присоединение воспаления
- Камнеобразование
- Формирование дивертикулов (выпячиваний стенки мочевого пузыря)
- Острая задержка мочи
- Развитие почечной недостаточности
Записаться на консультацию
Исследование пациентов с раком предстательной железы показало, что в 80% случаев развитие злокачественного процесса происходило на фоне длительно существовавшей доброкачественной гиперплазии предстательной железы.
Диагностика ДГПЖ
Диагноз ДГПЖ устанавливает врач-уролог на основании жалоб, анамнеза, врачебного урологического осмотра пациента и результатов обследования. Важное значение имеет точная информация о частоте мочеиспусканий и его объёме в течение суток (с указанием времени).
Важное значение имеет точная информация о частоте мочеиспусканий и его объёме в течение суток (с указанием времени).
Признаки гиперплазии простаты
- Трудности при мочеиспускании, вялая струя мочи
- Необходимость сделать усилие для начала мочеиспускания
- Ощущение неполного опорожнения мочевого пузыря, заставляющее мужчину неоднократно возвращаться в туалет
- Частые, настойчивые позывы к мочеиспусканию, в том числе в ночное время
Анализы и исследования
Общие клинические анализы крови и мочи
Биохимический анализ крови (мочевина, креатинин) – исключение/оценка почечной недостаточности
Определение уровня простат-специфического антигена (ПСА) в крови (маркёра воспаления и рака предстательной железы). ПСА при доброкачественной гиперплазии предстательной железы исследуется регулярно. Имеет значение уровень и темп нарастания ПСА.
Биопсия предстательной железы (при повышенном ПСА) для исключения/подтверждения рака простаты
Урофлоуметрия (измерение скорости потока мочи). Двукратная при выявлении отклонений.
Двукратная при выявлении отклонений.
Ультразвуковое исследование (УЗИ) почек и мочевыводящей системы, предстательной железы – трансабдоминальное и трансректальное (ТРУЗИ), в том числе исследование объёма остаточной мочи. Позволяет выявить/исключить мочекаменную болезнь, расширение чашечно-лоханочного аппарата, опухоли мочевыделителной системы, дивертикулы мочевого пузыря, оценить размеры, форму предстательной железы.
Эхопризнаки ДГПЖ (выявляемые при УЗИ)
- Увеличение объёма простаты до 20 и более см3.
- Неоднородная структура предстательной железы, наличие уплотнений (рубчиков), камней — кальцификатов (следов перенесенных воспалений), узловых образований.
- Объём остаточной мочи более 50 мл расценивается, как патологический.
Обзорная урография, экскреторная, ретроградная урография – рентгенологическое исследование мочевыделительной системы – почек, мочеточников, мочевого пузыря, уретры, в том числе с применением рентген-контрастного вещества. Оценка функции, строения мочевыводящей системы, положения почек и др.
Оценка функции, строения мочевыводящей системы, положения почек и др.
Стадии ДГПЖ
ДГПЖ 1 – стадия компенсации — предстательная железа 30 и более см3 в объёме, симптомы со стороны мочевого пузыря отсутствует или минимально выражены. Из-за небольшого сдавления мочеиспускательного канала мышца-детрузор в стенке мочевого пузыря гипертрофирована, но полностью справляется с его опорожнением.
ДГПЖ 2 – стадия субкомпенсации — простата увеличивается, сдавление уретры нарастает, мышечная стенка мочевого пузыря перестаёт справляться с полным изгнанием мочи, её гипертрофия сменяется гипотрофией, истончением. Неполное мочеиспускание — в мочевом пузыре остаётся >80 мл остаточной мочи. Затруднение отведения мочи вызывает её застой и расширение вышестоящих отделов – мочеточников, чашечек и лоханок почек. Постепенно развивается почечная недостаточность.
ДГПЖ 3 – стадия декомпенсации – невозможность опорожнить переполненный мочевой пузырь, так как его растянутая мышца-детрузор уже не способна к сокращению. В то же время происходит капельное подтекание мочи. Она самопроизвольно выдавливается по каплям из мочевого пузыря в уретру за счёт постоянного поступления из почек. Возникает реальная угроза острой задержки мочи – невозможности опорожнения мочевого пузыря при непреодолимом желании помочиться. Эта ситуация требует экстренной хирургической помощи.
В то же время происходит капельное подтекание мочи. Она самопроизвольно выдавливается по каплям из мочевого пузыря в уретру за счёт постоянного поступления из почек. Возникает реальная угроза острой задержки мочи – невозможности опорожнения мочевого пузыря при непреодолимом желании помочиться. Эта ситуация требует экстренной хирургической помощи.
Лечение ДГПЖ
Консервативное
- улучшение оттока мочи за счёт расслабления шейки мочевого пузыря, уретры,
- уменьшение размеров железы,
- улучшение состояния мышцы-детрузора мочевого пузыря.
Используется комбинированная фармакотерапия, которая подбирается индивидуально и корректируется по ходу лечения наблюдающим пациента урологом.
Хирургическое
При неэффективности консервативной терапии, прогрессировании ДГПЖ, выраженных расстройствах мочевыделения, нарастании объёма остаточной мочи, развитии осложнений (камнеобразования, гематурии – эритроцитов в моче, почечной недостаточности и др.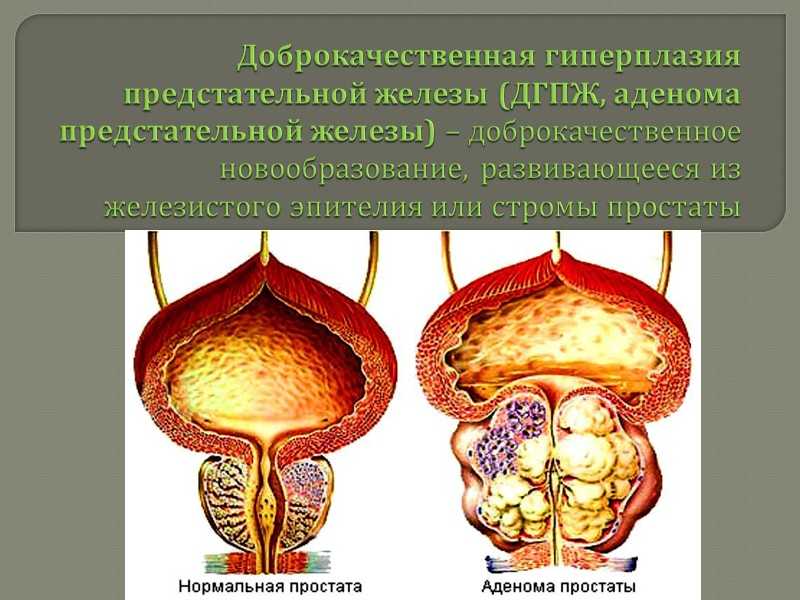 ) необходима операция.
) необходима операция.
Записаться на консультацию
В Клиническом госпитале на Яузе практикуется современный метод хирургического лечения аденомы предстательной железы – эндоскопическая лазерная вапоризация, при которой доступ к предстательной железе осуществляется через уретру, а избыточная ткань железы выпаривается лазером.
Литература:
-
Гориловский Л.М., Мирзоев К.М. Комбинированная терапия доброкачественной гиперплазии предстательной железы [Электронный ресурс] // Медицинский совет. 2011 https://cyberleninka.ru/article/n/kombinirovannaya-terapiya-dobrokachestvennoy-giperplazii-predstatelnoy-zhelezy -
Лобанов Д.В., Кириллов Ю.Б., Юдин В.А. Малоинвазивные методы в лечении доброкачественной гиперплазии предстательной железы [Электронный ресурс] // Российский медико-биологический вестник имени академика И. П. Павлова. 2001https://cyberleninka.ru/article/n/maloinvazivnye-metody-v-lechenii-dobrokachestvennoy-giperplazii-predstatelnoy-zhelezy
П. Павлова. 2001https://cyberleninka.ru/article/n/maloinvazivnye-metody-v-lechenii-dobrokachestvennoy-giperplazii-predstatelnoy-zhelezy
-
Доста Н.И, Вальвачев A.A. Доброкачественная гиперплазия предстательной железы: новый взгляд на этиопатогенез и лечение // БелМАПО. 2008 -
Коган М.И. Клинический разбор случая доброкачественной гиперплазии предстательной железы // РМЖ. 2011
Рак простаты: симптомы и признаки
Поиск
Утверждено редакционной коллегией Cancer.Net, 12/2022
НА ЭТОЙ СТРАНИЦЕ: Вы узнаете больше об изменениях и других вещах, которые могут сигнализировать о проблеме, которая может потребовать медицинской помощи. Используйте меню для просмотра других страниц.
Симптомы — это изменения, которые вы можете почувствовать в своем теле. Признаки — это изменения в чем-то измеряемом, например, при измерении артериального давления или выполнении лабораторного анализа. Вместе симптомы и признаки могут помочь описать медицинскую проблему. Хотя в большинстве случаев рак предстательной железы не вызывает никаких симптомов, симптомы и признаки рака предстательной железы могут включать:
Вместе симптомы и признаки могут помочь описать медицинскую проблему. Хотя в большинстве случаев рак предстательной железы не вызывает никаких симптомов, симптомы и признаки рака предстательной железы могут включать:
Частое мочеиспускание
Слабый или прерывистый поток мочи или необходимость натужиться, чтобы опорожнить мочевой пузырь
Частые позывы к мочеиспусканию ночью
Кровь в моче
Новое начало эректильной дисфункции
Боль или жжение во время мочеиспускания, что встречается гораздо реже
Дискомфорт или боль при сидении, вызванные увеличением предстательной железы
Другие доброкачественные состояния предстательной железы, такие как доброкачественная гипертрофия предстательной железы (ДГПЖ) или увеличенная предстательная железа, могут вызывать аналогичные симптомы. Или причиной симптома или признака может быть другое заболевание, также не связанное с раком. Мочевые симптомы также могут быть вызваны инфекцией мочевого пузыря или другими состояниями.
Мочевые симптомы также могут быть вызваны инфекцией мочевого пузыря или другими состояниями.
Если рак распространился за пределы предстательной железы, симптомы и признаки могут включать:
Боль в спине, бедрах, бедрах, плечах или других костях
Отек или скопление жидкости в ногах или ступнях
Необъяснимая потеря веса
Усталость
Изменение режима работы кишечника
Если вас беспокоят какие-либо изменения, которые вы испытываете, поговорите со своим врачом. Ваш врач спросит, как долго и как часто вы испытываете симптомы, в дополнение к другим вопросам. Это должно помочь выяснить причину проблемы, называемой диагностикой.
Если диагностирован рак, облегчение симптомов остается важной частью ухода и лечения рака. Управление симптомами можно назвать «паллиативным уходом» или «поддерживающим уходом». Его часто начинают вскоре после постановки диагноза и продолжают на протяжении всего лечения. Обязательно поговорите со своим лечащим врачом о симптомах, которые вы испытываете, включая любые новые симптомы или изменение симптомов.
Обязательно поговорите со своим лечащим врачом о симптомах, которые вы испытываете, включая любые новые симптомы или изменение симптомов.
Следующий раздел в этом руководстве называется Диагностика . В нем объясняется, какие анализы могут потребоваться, чтобы узнать больше о причине симптомов. Используйте меню, чтобы выбрать другой раздел для чтения в этом руководстве.
‹ Рак простаты – скрининг
вверх
Рак простаты — Диагностика ›
Своевременно. Надежный. Сострадательный.
Исчерпывающая информация для больных раком, их семей и лиц, осуществляющих уход, от Американского общества клинической онкологии (ASCO), голоса профессионалов в области онкологии со всего мира.
Find a Cancer Doctor
Особенности визуализации предстательной железы, указывающие на доброкачественную или злокачественную патологию при биопсии
1. Дикинсон Л., Ахмед Х.У., Аллен С. и соавт.
Магнитно-резонансная томография для обнаружения, локализации и характеристики рака предстательной железы: рекомендации европейского консенсусного совещания.
Евр Урол
2011;59:477-94. 10.1016/j.eururo.2010.12.009 [PubMed] [CrossRef] [Google Scholar]
2. Seo JW, Shin SJ, Taik Oh Y, et al.
PI-RADS, версия 2: Обнаружение клинически значимого рака у пациентов с раком предстательной железы с баллом по шкале Глисона 6 при биопсии.
AJR Am J Рентгенол
2017;209:П1-9. 10.2214/AJR.16.16981 [PubMed] [CrossRef] [Google Scholar]
3. Ploussard G, Epstein JI, Montironi R, et al.
Современная концепция значимого и незначительного рака предстательной железы.
Евр Урол
2011;60:291-303. 10.1016/j.eururo.2011.05.006 [PubMed] [CrossRef] [Google Scholar]
4. Ханахан Д., Вайнберг Р.А.
Отличительные признаки рака: следующее поколение.
Клетка
2011;144:646-74. 10.1016/j.cell.2011.02.013 [PubMed] [CrossRef] [Google Scholar]
5. Ahmed HU, Arya M, Freeman A, et al.
Имеют ли низкодифференцированные и малые объемы рака предстательной железы признаки злокачественности?
Ланцет Онкол
2012;13:e509-17.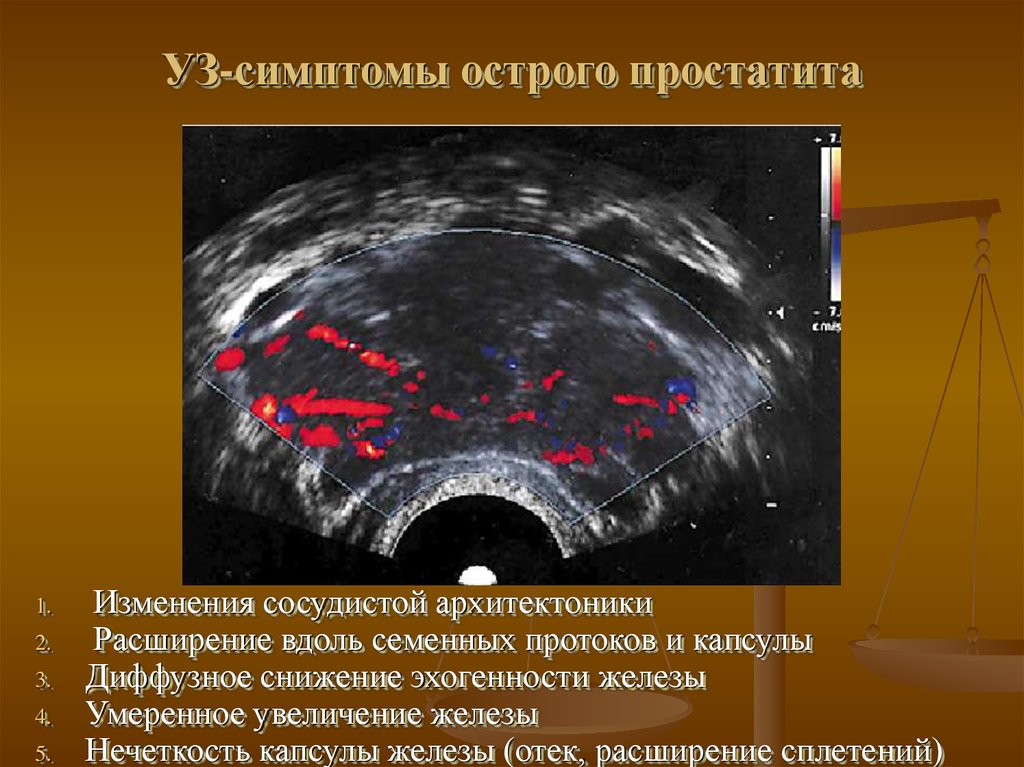 10.1016/S1470-2045(12)70388-1 [PubMed] [CrossRef] [Google Scholar]
10.1016/S1470-2045(12)70388-1 [PubMed] [CrossRef] [Google Scholar]
6. Gleason DF, Mellinger GT.
Прогнозирование прогноза аденокарциномы предстательной железы с помощью комбинированной гистологической классификации и клинической стадии.
Дж. Урол
1974; 111:58-64. 10.1016/S0022-5347(17)59889-4 [PubMed] [CrossRef] [Google Scholar]
7. Epstein JI, Allsbrook WC, Jr, Amin MB, et al.
Консенсусная конференция Международного общества урологической патологии (ISUP) 2005 г. по шкале Глисона для карциномы предстательной железы.
Ам Дж. Сург Патол
2005;29: 1228-42. 10.1097/01.pas.0000173646.99337.b1 [PubMed] [CrossRef] [Google Scholar]
8. Latour M, Amin MB, Billis A, et al.
Классификация инвазивной крибриформной карциномы по данным биопсии простаты: межнаблюдательное исследование среди экспертов в области патологии мочеполовой системы.
Ам Дж. Сург Патол
2008;32:1532-9. 10.1097/PAS.0b013e318169e8fd [PubMed] [CrossRef] [Google Scholar]
9. Danneman D, Drevin L, Robinson D, et al.
Инфляция Глисона 1998-2011: регистрационное исследование 97 168 мужчин.
БЖУ Интерн.
2015;115:248-55. 10.1111/bju.12671 [PubMed] [CrossRef] [Google Scholar]
10. Pierorazio PM, Walsh PC, Partin AW, et al.
Прогностическая группировка по Глисону: данные основаны на модифицированной системе подсчета баллов по Глисону.
БЖУ Интерн.
2013;111:753-60. 10.1111/j.1464-410X.2012.11611.x [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
11. Helpap B, Egevad L.
Значение модифицированной классификации Глисона карциномы предстательной железы в образцах биопсии и радикальной простатэктомии.
Арка Вирхова
2006;449:622-7. 10.1007/s00428-006-0310-6 [PubMed] [CrossRef] [Google Scholar]
12. Billis A, Quintal MM, Meirelles L, et al.
Значение модифицированной шкалы Глисона Международного общества урологической патологии (ISUP) 2005 года как предиктора биохимического рецидива после радикальной простатэктомии.
Инт Урол Нефрол
2014;46:935-40. 10.1007/s11255-013-0579-8 [PubMed] [CrossRef] [Google Scholar]
13. Pan CC, Potter SR, Partin AW, et al.
Pan CC, Potter SR, Partin AW, et al.
Прогностическое значение третичных паттернов Глисона более высокой степени в образцах радикальной простатэктомии: предложение изменить систему оценки Глисона.
Ам Дж. Сург Патол
2000;24:563-9. 10.1097/00000478-200004000-00011 [PubMed] [CrossRef] [Google Scholar]
14. D’Amico AV, Whittington R, Malkowicz SB, et al.
Биохимический исход после радикальной простатэктомии, дистанционной лучевой терапии или интерстициальной лучевой терапии при клинически локализованном раке предстательной железы.
ДЖАМА
1998; 280:969-74. 10.1001/jama.280.11.969 [PubMed] [CrossRef] [Google Scholar]
15. Epstein JI, Zelefsky MJ, Sjoberg DD, et al.
Современная система оценки рака простаты: проверенная альтернатива шкале Глисона.
Евр Урол
2016;69: 428-35. 10.1016/j.eururo.2015.06.046 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Wheeler TM, Dillioglugil O, Kattan MW, et al.
Клинико-патологическое значение уровня и степени капсулярной инвазии в клинической стадии Т1-2 рака предстательной железы.
Хум Патол
1998;29:856-62. 10.1016/S0046-8177(98)90457-9 [PubMed] [CrossRef] [Google Scholar]
17. Hull GW, Rabbani F, Abbas F, et al.
Контроль над раком с помощью только радикальной простатэктомии у 1000 последовательных пациентов.
Дж. Урол
2002;167:528-34. 10.1016/S0022-5347(01)69079-7 [PubMed] [CrossRef] [Google Scholar]
18. McNeal JE, Villers AA, Redwine EA, et al.
Гистологическая дифференциация, объем рака и метастазирование в тазовые лимфатические узлы при аденокарциноме предстательной железы.
Рак
1990;66:1225-33. 10.1002/1097-0142(19
5)66:6<1225::AID-CNCR2820660624>3.0.CO;2-X [PubMed] [CrossRef] [Google Scholar]
19. Stamey TA, Yemoto CE.
Исследование 3 молекулярных форм сывороточного специфического антигена простаты для различения отрицательной и положительной биопсии: отношение к объему переходной зоны.
Дж. Урол
2000;163:119-26. 10.1016/S0022-5347(05)67986-4 [PubMed] [CrossRef] [Google Scholar]
20. Stamey TA, Freiha FS, McNeal JE, et al.
Локализованный рак простаты. Отношение объема опухоли к клиническому значению для лечения рака предстательной железы.
Отношение объема опухоли к клиническому значению для лечения рака предстательной железы.
Рак
1993;71:933-8. 10.1002/1097-0142(19930201)71:3+<933::AID-CNCR2820711408>3.0.CO;2-L [PubMed] [CrossRef] [Google Scholar]
21. Bostwick DG, Graham SD, Jr, Napalkov П и др.
Стадирование раннего рака предстательной железы: предлагаемый прогностический индекс, основанный на объеме опухоли.
Урология
1993;41:403-11. 10.1016/0090-4295(93)90497-X [PubMed] [CrossRef] [Google Scholar]
22. Bonekamp D, Jacobs MA, El-Khouli R, et al.
Достижения в области МРТ предстательной железы: от диагностики к вмешательствам.
Рентгенография
2011;31:677-703. 10.1148/rg.313105139 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
23. Barrett T, Vargas HA, Akin O, et al.
Значение признака исключения кровоизлияния на Т1-взвешенных МРТ предстательной железы для выявления рака предстательной железы.
Радиология
2012; 263:751-7. 10.1148/radiol.12112100 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
24. Villers A, Lemaitre L, Haffner J, et al.
Villers A, Lemaitre L, Haffner J, et al.
Текущий статус МРТ для диагностики, определения стадии и прогноза рака предстательной железы: значение для фокальной терапии и активного наблюдения.
Курр Опин Урол
2009;19:274-82. 10.1097/MOU.0b013e328329a2ed [PubMed] [CrossRef] [Google Scholar]
25. Shah TT, To WKL, Ahmed HU.
Магнитно-резонансная томография в раннем выявлении рака предстательной железы и обзор литературы по клиническим путям, стратифицированным магнитно-резонансной томографией.
Эксперт Rev Anticancer Ther
2017;17:1159-68. 10.1080/14737140.2017.1383899 [PubMed] [CrossRef] [Google Scholar]
26. Wang L, Mazaheri Y, Zhang J, et al.
Оценка биологической агрессивности рака предстательной железы: корреляция интенсивности МР-сигнала со степенью Глисона после радикальной простатэктомии.
Радиология
2008; 246:168-76. 10.1148/radiol.2461070057 [PubMed] [CrossRef] [Google Scholar]
27. Weinreb JC, Barentsz JO, Choyke PL, et al.
PI-RADS Prostate Imaging — система отчетности и данных: 2015 г. , версия 2.
, версия 2.
Евр Урол
2016;69:16-40. 10.1016/j.eururo.2015.08.052 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
28. Hegde JV, Mulkern RV, Panych LP, et al.
Мультипараметрическая МРТ рака предстательной железы: обновленная информация о современных методах и их эффективности в обнаружении и локализации рака предстательной железы.
Резонансная визуализация J Magn
2013;37:1035-54. 10.1002/jmri.23860 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
29. Tamada T, Sone T, Higashi H, et al.
Выявление рака предстательной железы у пациентов с общим уровнем простатспецифического антигена в сыворотке крови 4–10 нг/мл: диагностическая эффективность диффузионно-взвешенной визуализации, динамической МРТ с контрастным усилением и Т2-взвешенной визуализации.
AJR Am J Рентгенол
2011;197:664-70. 10.2214/AJR.10.5923 [PubMed] [CrossRef] [Google Scholar]
30. Choyke PL, Dwyer AJ, Knopp MV.
Функциональная визуализация опухолей с помощью динамической магнитно-резонансной томографии с контрастным усилением.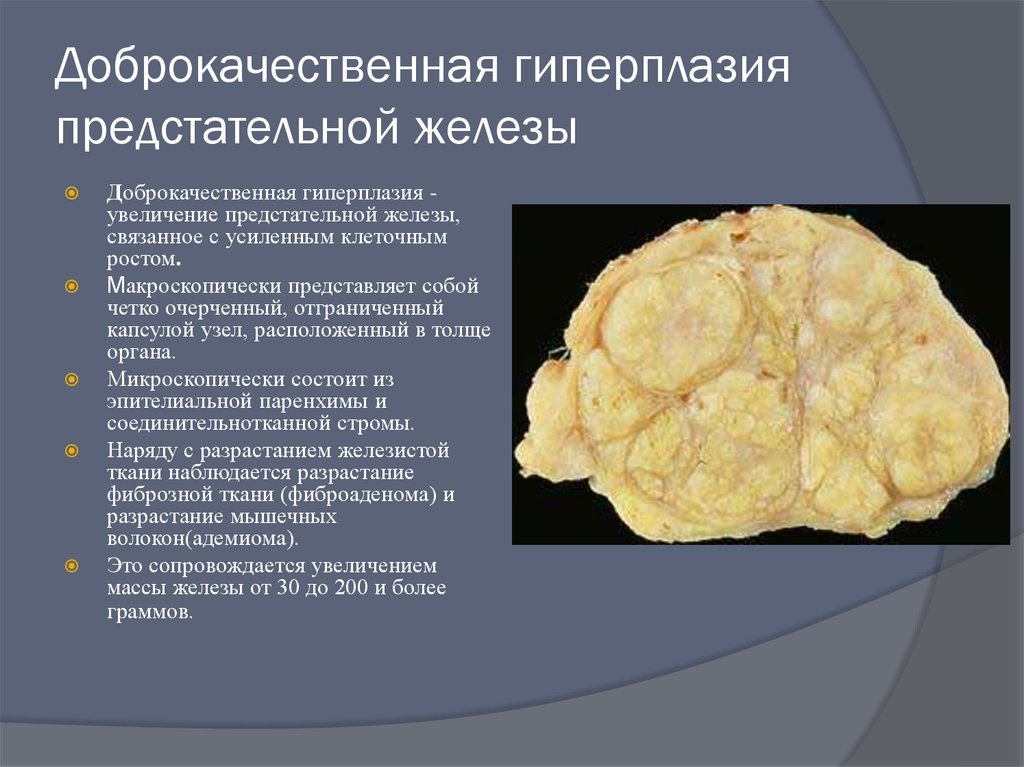
Резонансная визуализация J Magn
2003;17:509-20. 10.1002/jmri.10304 [PubMed] [CrossRef] [Google Scholar]
31. Zelhof B, Lowry M, Rodrigues G, et al.
Описание переменных усиления, полученных с помощью магнитно-резонансной томографии, при патологически подтвержденном раке предстательной железы и нормальных областях периферической зоны.
БЖУ Интерн.
2009 г.;104:621-7. 10.1111/j.1464-410X.2009.08457.x [PubMed] [CrossRef] [Google Scholar]
32. Futterer JJ, Heijmink SW, Scheenen TW, et al.
Локализация рака предстательной железы с помощью МРТ с динамическим контрастным усилением и протонной МРТ-спектроскопии.
Радиология
2006; 241:449-58. 10.1148/radiol.2412051866 [PubMed] [CrossRef] [Google Scholar]
33. Barentsz JO, Richenberg J, Clements R, et al.
Рекомендации по МРТ простаты ESUR 2012.
Евро Радиол
2012;22:746-57. 10.1007/s00330-011-2377-y [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
34. Barentsz JO, Weinreb JC, Verma S, et al.
Краткий обзор руководства PI-RADS v2 по мультипараметрической магнитно-резонансной томографии простаты и рекомендации по использованию.
Евр Урол
2016;69:41-9. 10.1016/j.eururo.2015.08.038 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Polanec S, Helbich TH, Bickel H, et al.
Непосредственное сравнение PI-RADS v2 и PI-RADS v1.
Евр Дж Радиол
2016;85:1125-31. 10.1016/j.ejrad.2016.03.025 [PubMed] [CrossRef] [Google Scholar]
36. Шин Т., Смит Т.Б., Укимура О. и соавт.
Диагностическая точность пятибалльной шкалы Лайкерта для магнитно-резонансной томографии (МРТ) оценивалась по результатам МРТ/ультразвуковой совмещенной прицельной биопсии предстательной железы.
БЖУ Интерн.
2018;121:77-83. 10.1111/bju.13972 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Harada T, Abe T, Kato F, et al.
Пятибалльная шкала Лайкерта на МРТ предсказывает клинически значимую карциному предстательной железы.
БМК Урол
2015;15:91. 10.1186/с12894-015-0087-5 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
38. Rosenkrantz AB, Lim RP, Haghighi M, et al.
Сравнение воспроизводимости интерридера системы отчетов и данных визуализации простаты и шкал Лайкерта для оценки многопараметрической МРТ простаты.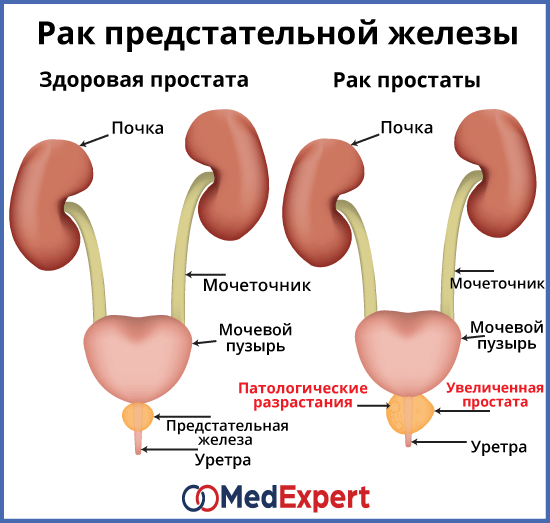
AJR Am J Рентгенол
2013;201:W612-8. 10.2214/AJR.12.10173 [PubMed] [CrossRef] [Google Scholar]
39. Hamoen EHJ, de Rooij M, Witjes JA, et al.
Использование системы отчетов и данных визуализации простаты (PI-RADS) для обнаружения рака простаты с помощью многопараметрической магнитно-резонансной томографии: диагностический метаанализ.
Евр Урол
2015;67:1112-21. 10.1016/j.eururo.2014.10.033 [PubMed] [CrossRef] [Google Scholar]
40. Ahmed HU, El-Shater Bosaily A, Brown LC, et al.
Диагностическая точность многопараметрической МРТ и биопсии ТРУЗИ при раке предстательной железы (ПРОМИС): парное валидирующее подтверждающее исследование.
Ланцет
2017;389:815-22. 10.1016/S0140-6736(16)32401-1 [PubMed] [CrossRef] [Google Scholar]
41. Kim CK, Park BK, Han JJ, et al.
Диффузионно-взвешенная визуализация предстательной железы при 3 Тл для дифференциации злокачественной и доброкачественной ткани в переходной и периферической зонах: предварительные результаты.
J Comput Assist Томогр
2007;31:449-54. 10.1097/01.rct.0000243456.00437.59 [PubMed] [CrossRef] [Google Scholar]
10.1097/01.rct.0000243456.00437.59 [PubMed] [CrossRef] [Google Scholar]
42. Tamada T, Sone T, Jo Y, et al.
Кажущиеся значения коэффициента диффузии в периферических и переходных зонах простаты: сравнение между нормальными и злокачественными тканями предстательной железы и корреляция с гистологической степенью.
Резонансная визуализация J Magn
2008;28:720-6. 10.1002/jmri.21503 [PubMed] [CrossRef] [Google Scholar]
43. Kim CK, Park BK, Lee HM, et al.
Значение диффузионно-взвешенной визуализации для прогнозирования локализации рака предстательной железы при 3T с использованием катушки с фазированной решеткой: предварительные результаты.
Инвест Радиол
2007;42:842-7. 10.1097/RLI.0b013e3181461d21 [PubMed] [CrossRef] [Google Scholar]
44. Пурыско А.С., Герц БР.
МРТ предстательной железы: признак исключения кровотечения.
Дж. Урол
2012; 188:1946-7. 10.1016/j.juro.2012.08.058 [PubMed] [CrossRef] [Google Scholar]
45. Американский колледж радиологии. ПИ-РАДС. Визуализация простаты – версия 2 системы отчетности и данных. Американский колледж радиологии. 2015. Доступно в Интернете: https://www.acr.org/-/media/ACR/Files/RADS/Pi-RADS/PIRADS-V2.pdf?la=en. Дата обращения 03.02.2018 2018.
Американский колледж радиологии. 2015. Доступно в Интернете: https://www.acr.org/-/media/ACR/Files/RADS/Pi-RADS/PIRADS-V2.pdf?la=en. Дата обращения 03.02.2018 2018.
46. Kitzing YX, Prando A, Varol C, et al.
Доброкачественные состояния, имитирующие карциному предстательной железы: особенности МРТ с гистопатологической корреляцией.
Рентгенография
2016;36:162-75. 10.1148/rg.2016150030 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
47. Rais-Bahrami S, Nix JW, Turkbey B, et al.
Клинические и мультипараметрические МРТ-признаки гранулематозного простатита.
Брюшной Радиол (Нью-Йорк)
2017;42:1956-62. 10.1007/s00261-017-1080-0 [PubMed] [CrossRef] [Google Scholar]
48. Bour L, Schull A, Delongchamps NB, et al.
Мультипараметрические МРТ-признаки гранулематозного простатита и туберкулезного абсцесса предстательной железы.
Диагностическая визуализация
2013;94:84-90. 10.1016/j.diii.2012.09.001 [PubMed] [CrossRef] [Google Scholar]
49. Прандо А., Биллис А.
Очаговая атрофия предстательной железы: имитация рака предстательной железы при ТРУЗИ и 3D-МРСИ.
Визуализация брюшной полости
2009;34:271-5. 10.1007/s00261-008-9382-x [PubMed] [CrossRef] [Google Scholar]
50. Litjens GJS, Elliott R, Shih NN, et al.
Компьютерные признаки могут отличить доброкачественное смешанное заболевание от аденокарциномы предстательной железы при мультипараметрической МРТ.
Радиология
2016; 278:135-45. 10.1148/radiol.2015142856 [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Panebianco V, Barchetti F, Barentsz J, et al.
Подводные камни в интерпретации мп-МРТ простаты: иллюстрированный обзор с патологической корреляцией.
Инсайты
2015;6:611-30. 10.1007/s13244-015-0426-9 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Peng Y, Jiang Y, Yang C, et al.
Количественный анализ многопараметрических МРТ-изображений предстательной железы: дифференциация между раком предстательной железы и нормальной тканью и корреляция с оценкой Глисона — компьютерное исследование развития диагностики.
Радиология
2013;267:787-96. 10.1148/radiol.13121454 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
53. Panagiotaki E, Walker-Samuel S, Siow B, et al.
Неинвазивная количественная оценка микроструктуры солидной опухоли с помощью VERDICT MRI.
Рак Рез
2014;74:1902-12. 10.1158/0008-5472.CAN-13-2511 [PubMed] [CrossRef] [Google Scholar]
54. Panagiotaki E, Chan RW, Dikaios N, et al.
Микроструктурная характеристика нормальной и злокачественной ткани предстательной железы человека с сосудистой, внеклеточной и ограниченной диффузией для цитометрии при магнитно-резонансной томографии опухолей.
Инвест Радиол
2015;50:218-27. 10.1097/RLI.0000000000000115 [PubMed] [CrossRef] [Google Scholar]
55. Bratan F, Melodelima C, Souchon R, et al.
Насколько точна мультипараметрическая МРТ при оценке объема рака предстательной железы?
Радиология
2015; 275:144-54. 10.1148/radiol.14140524 [PubMed] [CrossRef] [Google Scholar]
56. Coakley FV, Kurhanewicz J, Lu Y, et al.
Объем опухоли рака предстательной железы: измерение с помощью эндоректальной МРТ и МРТ-спектроскопии.
Радиология
2002; 223:91-7. 10.1148/radiol.2231010575 [PubMed] [CrossRef] [Google Scholar]
57. Langer DL, van der Kwast TH, Evans AJ, et al.
Смешанная нормальная ткань в раке предстательной железы: влияние на измерения МРТ кажущегося коэффициента диффузии и T2 — разреженный рак по сравнению с плотным.
Радиология
2008; 249:900-8. 10.1148/radiol.2493080236 [PubMed] [CrossRef] [Google Scholar]
58. Le Nobin J, Rosenkrantz AB, Villers A, et al.
Фокусная терапия с визуальным контролем для видимого рака предстательной железы с помощью магнитно-резонансной томографии: определение трехмерного поля лечения на основе анализа совместной регистрации магнитно-резонансной томографии.
Дж. Урол
2015;194:364-70. 10.1016/j.juro.2015.02.080 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Testa C, Pultrone C, Manners DN, et al.
Метаболическая визуализация при раке простаты: где мы находимся.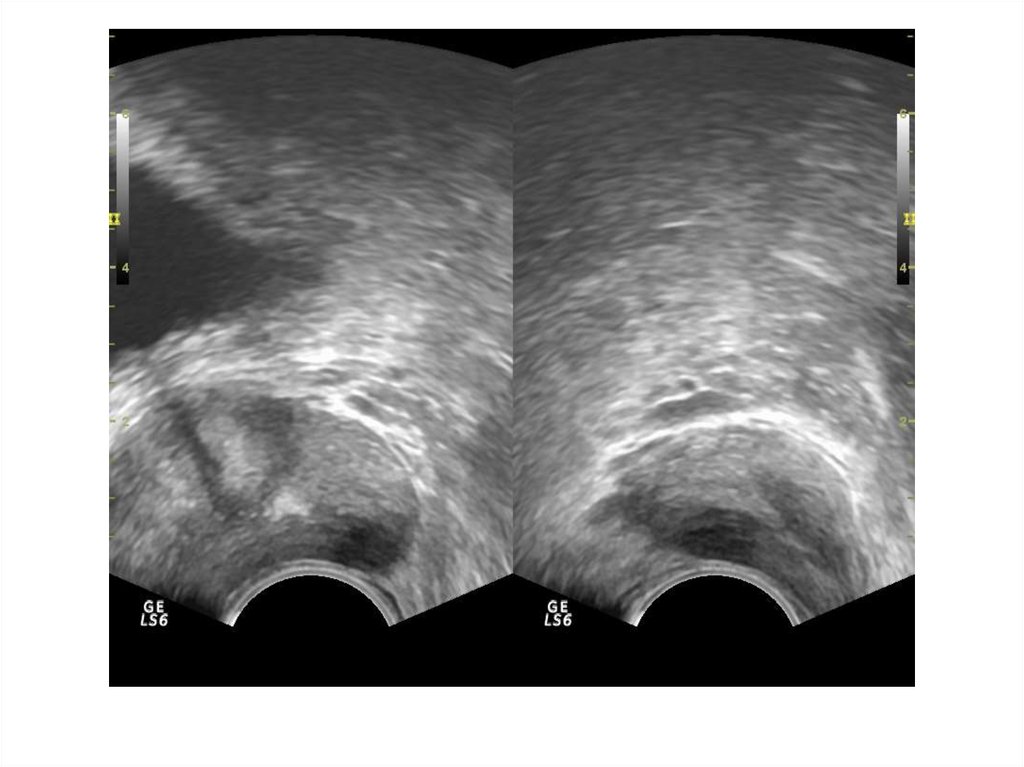
Фронт Онкол
2016;6:225. 10.3389/fonc.2016.00225 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
60. Scheenen TW, Rosenkrantz AB, Haider MA, et al.
Мультипараметрическая магнитно-резонансная томография в лечении рака предстательной железы: текущее состояние и перспективы на будущее.
Инвест Радиол
2015;50:594-600. 10.1097/RLI.0000000000000163 [PubMed] [CrossRef] [Google Scholar]
61. Scheenen TW, Futterer J, Weiland E, et al.
Отличие рака от нераковой ткани в предстательной железе с помощью трехмерной протонной магнитно-резонансной спектроскопии: проспективное многоцентровое проверочное исследование.
Инвест Радиол
2011;46:25-33. 10.1097/RLI.0b013e3181f54081 [PubMed] [CrossRef] [Google Scholar]
62. Fusco R, Sansone M, Petrillo M, et al.
Мультипараметрическая МРТ для обнаружения рака предстательной железы: предварительные результаты количественного анализа динамической контрастной визуализации, диффузионно-взвешенной визуализации и спектроскопии.
Магнитно-резонансная визуализация
2016;34:839-45. 10.1016/j.mri.2016.04.001 [PubMed] [CrossRef] [Google Scholar]
10.1016/j.mri.2016.04.001 [PubMed] [CrossRef] [Google Scholar]
63. Shukla-Dave A, Hricak H, Eberhardt SC, et al.
Хронический простатит: результаты МРТ и 1H МР-спектроскопии — первоначальные наблюдения.
Радиология
2004; 231:717-24. 10.1148/radiol.2313031391 [PubMed] [CrossRef] [Google Scholar]
64. Hovels AM, Heesakkers RA, Adang EM, et al.
Диагностическая точность КТ и МРТ при стадировании тазовых лимфатических узлов у больных раком предстательной железы: метаанализ.
Клин Радиол
2008;63:387-95. 10.1016/j.crad.2007.05.022 [PubMed] [CrossRef] [Google Scholar]
65. Effert PJ, Bares R, Handt S, et al.
Метаболическая визуализация нелеченного рака предстательной железы с помощью позитронно-эмиссионной томографии с дезоксиглюкозой, меченной 18-фтором.
Дж. Урол
1996; 155:994-8. 10.1016/S0022-5347(01)66366-3 [PubMed] [CrossRef] [Google Scholar]
66. Европейская ассоциация урологов. Рак простаты. Европейская ассоциация урологов. 2018. Доступно онлайн: http://uroweb. org/guideline/prostate-cancer/. Дата обращения 05.02.20192018.
org/guideline/prostate-cancer/. Дата обращения 05.02.20192018.
67. Evangelista L, Guttilla A, Zattoni F, et al.
Полезность холиновой позитронно-эмиссионной томографии/компьютерной томографии для выявления поражения лимфатических узлов при раке предстательной железы от среднего до высокого риска: систематический обзор литературы и метаанализ.
Евр Урол
2013;63:1040-8. 10.1016/j.eururo.2012.09.039 [PubMed] [CrossRef] [Google Scholar]
68. Afshar-Oromieh A, Avtzi E, Giesel FL, et al.
Диагностическая ценность ПЭТ/КТ-изображения с (68)Ga-меченым лигандом PSMA HBED-CC в диагностике рецидивирующего рака предстательной железы.
Eur J Nucl Med Mol Imaging
2015;42:197-209. 10.1007/s00259-014-2949-6 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
69. Maurer T, Eiber M, Schwaiger M, et al.
Текущее использование PSMA-PET в лечении рака предстательной железы.
Нат Рев Урол
2016;13:226-35. 10.1038/nrurol.2016.26 [PubMed] [CrossRef] [Google Scholar]
70. Silver DA, Pellicer I, Fair WR, et al.
Экспрессия простатспецифического мембранного антигена в нормальных и злокачественных тканях человека.
Клин Рак Рез
1997;3:81-5. [PubMed] [Google Scholar]
71. Милоушев В.З., Кешари К.Р., Холодный А.И.
МРТ с гиперполяризацией: доклинические модели и возможные применения в нейрорадиологии.
Резонансная визуализация с верхним магнитным полем
2016;25:31-7. 10.1097/RMR.0000000000000076 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
72. Nelson SJ, Kurhanewicz J, Vigneron DB, et al.
Метаболическая визуализация пациентов с раком предстательной железы с использованием гиперполяризованного [1-(1)(3)C]пирувата.
Sci Transl Med
2013;5:198ra108. 10.1126/scitranslmed.3006070 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
73. Aggarwal R, Vigneron DB, Kurhanewicz J.
Магнитно-резонансная томография с гиперполяризованным 1-[(13)C]-пируватом выявляет ранний метаболический ответ на андрогенную абляцию при раке предстательной железы.
Евр Урол
2017;72:1028-9. 10.1016/j.eururo.2017.07.022 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
10.1016/j.eururo.2017.07.022 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
74. Kurhanewicz J, Vigneron DB, Brindle K, et al.
Анализ метаболизма рака с помощью визуализации гиперполяризованных ядер: перспективы перевода в клинические исследования.
Неоплазия
2011;13:81-97. 10.1593/neo.101102 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
75. Klotz L, Emberton M.
Лечение рака предстательной железы низкого риска: активное наблюдение и фокальная терапия.
Курр Опин Урол
2014;24:270-9. 10.1097/MOU.0000000000000055 [PubMed] [CrossRef] [Google Scholar]
76. Muthigi A, George AK, Sidana A, et al.
Отсутствие цели: модернизация рака предстательной железы с помощью систематической биопсии вместо магнитно-резонансной томографии / трансректальной ультразвуковой комбинированной биопсии.
Дж. Урол
2017;197:327-34. 10.1016/j.juro.2016.08.097 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
77. Filson CP, Natarajan S, Margolis DJ, et al.
Выявление рака предстательной железы с помощью магнитно-резонансной и ультразвуковой биопсии: роль систематических и целевых биопсий.
Рак
2016;122:884-92. 10.1002/cncr.29874 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
78. Hansen NL, Barrett T, Koo B, et al.
Влияние плотности простат-специфического антигена на положительные и отрицательные прогностические значения мультипараметрической магнитно-резонансной томографии для выявления рака предстательной железы 7-10 баллов по шкале Глисона при повторной биопсии.
БЖУ Интерн.
2017;119:724-30. 10.1111/bju.13619 [PubMed] [CrossRef] [Google Scholar]
79. Abdi H, Zargar H, Goldenberg SL, et al. Мультипараметрическая магнитно-резонансная томография для выявления рака предстательной железы у пациентов с отрицательными результатами биопсии в анамнезе. Урол Онкол 2015;33:165 e1-7. [ПубМед]
80. Venderink W, van Luijtelaar A, Bomers JG, et al. Результаты прицельной биопсии у мужчин с поражениями магнитно-резонансной томографии, классифицированными как сомнительные, вероятные или с высокой вероятностью клинически значимого рака простаты.


 Должна прослеживаться визуализация семенных пузырьков, а диаметр составлять не более 25 мм. Но, так бывает не всегда.
Должна прослеживаться визуализация семенных пузырьков, а диаметр составлять не более 25 мм. Но, так бывает не всегда. Патологию не трудно распознать по анализу на гормоны и УЗИ.
Патологию не трудно распознать по анализу на гормоны и УЗИ. На УЗИ будет заметно увеличение простаты, зональная эхогенность и тканевых уплотнения для хронической формы.
На УЗИ будет заметно увеличение простаты, зональная эхогенность и тканевых уплотнения для хронической формы.

 Надеемся, статья помогла вам получше узнать о структурных диффузных изменениях предстательной железы, что это такое, и какие действия необходимо совершить для лечения недуга.
Надеемся, статья помогла вам получше узнать о структурных диффузных изменениях предстательной железы, что это такое, и какие действия необходимо совершить для лечения недуга. П. Павлова. 2001https://cyberleninka.ru/article/n/maloinvazivnye-metody-v-lechenii-dobrokachestvennoy-giperplazii-predstatelnoy-zhelezy
П. Павлова. 2001https://cyberleninka.ru/article/n/maloinvazivnye-metody-v-lechenii-dobrokachestvennoy-giperplazii-predstatelnoy-zhelezy