Сдать анализы — Тестостерон свободный, цена анализа в СПБ
Свободный тестостерон – биологически активная фракция стероидного полового гормона тестостерона, не связанная с белками крови.
Услуги по взятию (сбору) биоматериала
Венозная кровь
Срок выполнения
до 5 суток
Влияние лекарственных препаратов
Ингибиторы продукции гонадотропных гормонов
-
Даназол (Повышает значение)
Синонимы русские
Тестостерон прямой.
Синонимы английские
Testosterone Free, Testosterone Direct, Unbound Testosterone.
Метод исследования
Иммуноферментный анализ (ИФА).
Единицы измерения
Пг/мл (пикограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
-
Не принимать пищу в течение 12 часов перед анализом.
-
Исключить прием эстрогенов, андрогенов за 48 часов до исследования. -
При отсутствии особых указаний врача кровь на анализ рекомендуется сдавать до 11 часов утра. -
Исключить физическое и эмоциональное перенапряжение за 30 минут до исследования. -
Не курить в течение 30 минут до сдачи крови.
Общая информация об исследовании
Тестостерон – стероидный гормон из группы андрогенов (мужских половых гормонов). У мужчин вырабатывается клетками Лейдига в яичках и в небольшом количестве в коре надпочечников, у женщин — в яичниках и надпочечниках. Основными функциями тестостерона являются контроль над правильным развитием мужских половых органов, увеличение объема скелетных мышц, стимуляция сперматогенеза, роста волос на кожных покровах в области лица, подмышечных впадин, лобка. Секреция гормона меняется с возрастом – нарастает до 30 лет, а после 50 начинает снижаться. Также отмечаются и суточные колебания тестостерона: пик между 4 и 8 часами утра и минимум между 16 и 20 часами вечера.
При избыточном образовании андрогенов у женщин возникает вирилизация (вторичные половые признаки, характерные для мужчин), гирсутизм (чрезмерное оволосение по мужскому типу), огрубение голоса, гипертрофия клитора. Так как тестостерон стимулирует функцию сальных желез, его повышение часто связывают с развитием угревой сыпи. Сниженный синтез тестостерона у мужчин ведет к гипогонадизму (недоразвитию половых желез), оволосению по женскому типу, слабому развитию скелетной мускулатуры, недоразвитию наружных половых органов, бесплодию, увеличению молочных желез, ожирению. Недостаточная продукция данного андрогена у пожилых мужчин увеличивает риск остеопороза.
Общий тестостерон крови делится на 3 вида: тестостерон свободный (не связанный с белком, 1-4 % от общего), тестостерон, соединенный с глобулином, связывающим половые гормоны (60-70 %), и тестостерон, связанный с альбумином (слабосвязанный тестостерон, 25-40 %). Свободная и слабосвязанная формы – это биодоступный тестостерон, то есть обладающий биологической активностью. Связанный тестостерон, в свою очередь, не является активным.
Связанный тестостерон, в свою очередь, не является активным.
Уровень свободного тестостерона не зависит от изменений концентрации глобулина, связывающего половые гормоны (ГСПГ). Поэтому, если ГСПГ повышен (при гипертиреоидизме, циррозе, приеме пероральных контрацептивов и противоэпилептических средств, гиперэстрогенных состояниях, в том числе беременности) или снижен (при гипотиреоидизме, ожирении, избытке андрогенов, нефритическом синдроме), тест на свободный тестостерон будет более информативным, чем на общий.
Для чего используется исследование?
-
Для выявления причин раннего полового созревания или задержки полового развития у мальчиков. -
Для выявления причин импотенции и бесплодия у мужчин. -
Для диагностики тестостеронпродуцирующих опухолей половых желез. -
Для выявления поликистоза яичников и других причин вирилизации у женщин. -
Для контроля за лечением рака простаты аналогами гонадолиберинов и антиандрогенами.
-
Для выявления причин угревой сыпи. -
Для диагностики гипоталамо-гипофизарных нарушений, оценки функции эндокринной системы организма. -
Для уточнения пола новорожденных с неоднозначными половыми признаками.
Когда назначается исследование?
Мужчинам:
-
при задержке развития вторичных половых признаков или раннем половом созревании, -
при снижении полового влечения и сексуальных функций, импотенции, -
при подозрении на гипогонадизм, -
при бесплодии, -
при андропаузе («мужской менопаузе»), -
при выраженной угревой сыпи, -
при остеопорозе.
Женщинам:
-
при нерегулярном менструальном цикле или при отсутствии менструации, -
при бесплодии, -
при гирсутизме и/или чрезмерном развитии мужских внешних признаков, облысении, -
при угревой сыпи.
Новорожденным с неоднозначными половыми признаками анализ может быть назначен вместе с определением уровня других половых гормонов и инструментальными методами диагностики.
Что означают результаты?
Референсные значения
Для тест-системы Free Testosterone ELISA (EIA-2924), DRG:
|
|
|
|
|
|
|
|
|
|
| |
|
|
| |
|
|
| |
|
|
|
|
|
|
| |
|
|
| |
|
|
|
Для тест-системы Free Testosterone (CAN-fTE-260), Diagnostics Biochem Canada Inc. :
:
|
|
|
|
|
|
|
|
|
Причины повышения уровня тестостерона свободного
У мужчин:
-
опухоли яичек и надпочечников, -
врожденная гиперплазия и дисфункция коры надпочечников (сопровождает дефицит ферментов 21- или 11-гидроксилазы), -
раннее половое созревание у мальчиков, -
синдром Иценко – Кушинга, -
синдром Рейфенштейна.
У женщин:
-
синдром поликистозных яичников, -
опухоль яичников, эндометрия и надпочечников, -
адреногенитальный синдром (врожденная гиперплазия коры надпочечников), -
синдром Иценко – Кушинга.
Причины понижения уровня тестостерона свободного
У мужчин:
-
генетические нарушения полового развития и производства тестостерона (синдром Клайнфелтера, синдром Прадера – Вилли), -
патология гипоталамо-гипофизарной системы, связанная с продукцией лютеинизирующего гормона, -
патология яичек (крипторхизм, миотоническая дистрофия), -
приобретенная патология половых желез (из-за травмы яичек, перенесенного, как при вирусном паротите, лучевого поражения или токсического воздействия этанола при алкоголизме), -
прием аналогов гонадолиберинов или антиандрогенов, -
пожилой возраст.
У женщин снижение свободного тестостерона в клинической практике не принимают во внимание.
Что может влиять на результат?
Лекарственные препараты, повышающие уровень тестостерона: противосудорожные средства, барбитураты, бромокриптин, кломифен, даназол, эстрогены, миноксидил, правастатин, рифампицин, тамоксифен, бикалютамид, касодекс, циметидин, финастерид, люпрон, нилютамид, анаболические стероиды, гозерелин, левоноргестрел, нафарелин, налоксон, мифепристон, пероральные контрацептивы, фенитоин, вальпроевая кислота.
Лекарственные препараты, понижающие уровень тестостерона: антиандрогены, карбамазепин, кортикостероиды, циклофосфамид, дигоксин, эстрадиола валерат, фолликулостимулирующий гормон, финастерид, гемфиброзил, интерлейкин, кетоконазол, леупролид, магнезия, наркотические препараты, нафарелин, станозолол, спиронолактон, тетрациклин, верапамил, ципротерон, диэтилстильбэстрол, глюкоза, этанол, галотан, метопролол, метирапон, фенотиазиды.
После физических нагрузок уровень тестостерона в крови увеличивается.
Важные замечания
-
Результаты анализа необходимо интерпретировать с учетом возраста и пола пациента. -
У мужчин уровень гормона изменяется в течение суток, достигая максимума в 4.00-8.00 часов и минимума в 16.00-20.00. -
У женщин уровень тестостерона выше всего в середине цикла. -
Концентрация тестостерона в крови постепенно уменьшается с возрастом.
Также рекомендуется
-
Тестостерон -
Глобулин, связывающий половые гормоны (ГСПГ) -
Фолликулостимулирующий гормон (ФСГ) -
Лютеинизирующий гормон (ЛГ) -
Эстрадиол -
Прогестерон -
Пролактин -
Дигидротестостерон -
Дегидроэпиандростерон-сульфат (ДЭА-SO4) -
Антитела к стероидпродуцирующим клеткам яичка -
Ингибин B -
Антимюллеровский гормон -
Андростендион -
17-гидроксипрогестерон (17-ОПГ) -
17-кетостероиды (17-КС) в моче (развернутый) -
Спермограмма -
Гормонозависимое нарушение сперматогенеза -
Генетические причины мужского бесплодия
Кто назначает исследование?
Эндокринолог, гинеколог, андролог, уролог, репродуктолог.
Тип биоматериала и способы взятия
|
|
|
|
|
|
|
|
|
На дому: возможно взятие биоматериала сотрудником мобильной службы.
В Диагностическом центре: взятие, либо самостоятельный сбор биоматериала осуществляется в Диагностическом центре.
Самостоятельно: сбор биоматериала осуществляется самим пациентом (моча, кал, мокрота и т. п.). Другой вариант – образцы биоматериала предоставляет пациенту врач (например, операционный материал, ликвор, биоптаты и т.п.). После получения образцов пациент может как самостоятельно доставить их в Диагностический центр, так и вызвать мобильную службу на дом для передачи их в лабораторию.
п.). Другой вариант – образцы биоматериала предоставляет пациенту врач (например, операционный материал, ликвор, биоптаты и т.п.). После получения образцов пациент может как самостоятельно доставить их в Диагностический центр, так и вызвать мобильную службу на дом для передачи их в лабораторию.
Литература
-
Fischbach F.T., Dunning M.B. A Manual of Laboratory and Diagnostic Tests, 8th Ed. Lippincott Williams & Wilkins, 2008: 1344pp -
Fisher D.A. The Quest diagnostics manual. Endocrinology test selection and interpretation, 4th ed. San Juan Capistrano, CA: Quest Diagnostics Nichols Institute, 2007:369pp -
Wilson D. McGraw-Hill Manual of Laboratory and Diagnostic Tests 1st Ed Normal, Illinois, 2007:366pp -
Н. Лавин (ред.). Эндокринология.
Влияние тестостерона на соматическое здоровье мужчин | Гамидов С.И., Овчинников Р.И., Попова А.Ю.
Клинические проявления снижения активности половых гормонов у мужчин, в настоящее время называемого мужским гипогонадизмом, хорошо известны с глубокой древности. Они включают в себя утрату полового влечения и эректильной функции, уменьшение мышечной массы и силы, изменения настроения и характера оволосения. Однако в течение последних 20 лет стали накапливаться сведения о том, что последствия гипогона-дизма не ограничиваются изложенными выше изменениями. В частности, существует целый ряд доказательств существования связи между гипогонадизмом и заболеваниями сердечно-сосудистой системы (ССС). Рассмотрению данного вопроса и посвящена настоящая работа.
Они включают в себя утрату полового влечения и эректильной функции, уменьшение мышечной массы и силы, изменения настроения и характера оволосения. Однако в течение последних 20 лет стали накапливаться сведения о том, что последствия гипогона-дизма не ограничиваются изложенными выше изменениями. В частности, существует целый ряд доказательств существования связи между гипогонадизмом и заболеваниями сердечно-сосудистой системы (ССС). Рассмотрению данного вопроса и посвящена настоящая работа.
На протяжении длительного времени было принято считать, что тестостерон оказывает неблагоприятное действие на вероятность развития и течение болезней ССС. Эта точка зрения была основана прежде всего на том, что мужчины чаще страдают подобными заболеваниями. Кроме того, известно, что эстрогены, исторически рассматриваемые в качестве антагонистов андрогенов, снижают риск развития сердечно-сосудистых нарушений у женщин. Последнее, в частности, доказывают ростом числа таких заболеваний после менопаузы.
В последние годы данная позиция подвергается серьезному пересмотру [1]. Методически верно выполненные исследования не подтвердили взаимосвязи между уровнем тестостерона в крови и сердечно-сосудистыми заболеваниями (ССЗ) у мужчин [2, 3]. В некоторых работах даже было показано, что более высокая концентрация гормона может обладать благоприятным эффектом [4, 5]. Лечение препаратами тестостерона также не сопровождается повышением частоты инфарктов миокарда, стенокардии или инсультов [6, 7], более того, предполагается снижение вероятности этих осложнений [8, 9]. В ряде работ показано также, что уровень тестостерона в крови у мужчин обратно связан со смертностью как от ССЗ, так и от всех причин в целом [10–12].
Природа отрицательного влияния снижения уровня тестостерона на развитие ССЗ окончательно не установлена. Тем не менее существующие данные указывают на то, что неблагоприятное действие гипогонадиз-ма на ССС может осуществляться посредством метаболического синдрома (МС). Последний является хорошо известной комбинацией различных факторов сосудистого риска, в т. ч. нарушения толерантности к глюкозе, ожирения, артериальной гипертензии и дислипидемии. Риск развития МС у пациентов с гипогонадизмом значительно повышен [13–15]. Эти данные настолько убедительны, что было даже высказано предположение о целесообразности включения гипогонадизма в число критериев диагностики МС [13]. В то же время продолжается изучение вопросов, возникающих после изучения этих эпидемиологических данных. Что является причиной и что следствием: компоненты МС приводят к подавлению функции яичек или гипогонадизм способствует их развитию? Каковы механизмы этих взаимосвязей? Однозначного ответа на эти вопросы все еще не получено. Наиболее вероятным является существование двунаправленной связи между гипогонадизмом и МС.
Последний является хорошо известной комбинацией различных факторов сосудистого риска, в т. ч. нарушения толерантности к глюкозе, ожирения, артериальной гипертензии и дислипидемии. Риск развития МС у пациентов с гипогонадизмом значительно повышен [13–15]. Эти данные настолько убедительны, что было даже высказано предположение о целесообразности включения гипогонадизма в число критериев диагностики МС [13]. В то же время продолжается изучение вопросов, возникающих после изучения этих эпидемиологических данных. Что является причиной и что следствием: компоненты МС приводят к подавлению функции яичек или гипогонадизм способствует их развитию? Каковы механизмы этих взаимосвязей? Однозначного ответа на эти вопросы все еще не получено. Наиболее вероятным является существование двунаправленной связи между гипогонадизмом и МС.
Инсулинорезистентность (ИР), ведущий патофизиологический механизм развития МС и его осложнений, коррелирует с уровнем тестостерона в крови [16]. Пациенты с гипогонадизмом характеризуются более низкой чувствительностью к действию инсулина. Есть основания полагать, что гипогонадизм способствует развитию ИР В частности, признаки резистентности к действию инсулина выявлены как в экспериментальной модели гипогонадизма [17], так и у мужчин с синдромом Клайнфельтера [18]. Кроме того, развитие изменений, характерных для МС, включая ИР, дислипидемию и ожирение, имеет место на фоне острого гипогонадизма, вызванного медикаментозной терапией [19]. Подобная ситуация имеет место, в частности, при лечении рака предстательной железы (РПЖ) препаратами из группы аналогов гонадотропин-рилизинг гормона.
Есть основания полагать, что гипогонадизм способствует развитию ИР В частности, признаки резистентности к действию инсулина выявлены как в экспериментальной модели гипогонадизма [17], так и у мужчин с синдромом Клайнфельтера [18]. Кроме того, развитие изменений, характерных для МС, включая ИР, дислипидемию и ожирение, имеет место на фоне острого гипогонадизма, вызванного медикаментозной терапией [19]. Подобная ситуация имеет место, в частности, при лечении рака предстательной железы (РПЖ) препаратами из группы аналогов гонадотропин-рилизинг гормона.
Значительный интерес также представляет связь между гипогонадизмом и сахарным диабетом (СД) 2-го типа. Данный вопрос изучают уже достаточно долго, и накоплен ряд важных сведений, многие из которых актуальны в контексте рассматриваемой проблемы. В частности, мужчины, страдающие СД 2-го типа, не только чаще имеют пониженный уровень тестостерона в крови [20], но наличие последнего у здоровых мужчин является прогностическим фактором развития у них СД в будущем [14]. Кроме того, применение препаратов тестостерона больными СД 2-го типа сопровождается снижением выраженности ИР и улучшением контроля над уровнем глюкозы в крови [21]. Точный механизм развития подобных благоприятных эффектов тестостерона не установлен, но рассматривается возможность того, что он связан с изменениями конституции, прежде всего в форме снижения объема жировой ткани.
Кроме того, применение препаратов тестостерона больными СД 2-го типа сопровождается снижением выраженности ИР и улучшением контроля над уровнем глюкозы в крови [21]. Точный механизм развития подобных благоприятных эффектов тестостерона не установлен, но рассматривается возможность того, что он связан с изменениями конституции, прежде всего в форме снижения объема жировой ткани.
В то же время гиперинсулинемия может оказывать подавляющее действие на эндокринную функцию яичек[22]. Кроме того, показано, что подавление секреции инсулина приводит к повышению концентрации белка, связывающего в крови половые гормоны [23]. Это в свою очередь вызывает снижение биологической активности тестостерона. Подавление инсулином синтеза данного белка подтверждено в экспериментальных условиях [24]. В целом вопрос о влиянии инсулина на синтез тестостерона все еще далек от своего разрешения. Можно предполагать, что различные отклонения в синтезе инсулина могут, хотя и по-разному, но негативно отражаться на биологической активности тестостерона.
Существование обратной связи между объемом жировой ткани и уровнем тестостерона в крови подтверждено во многих исследованиях [25, 26]. Эта взаимосвязь, по-видимому, носит комплексный характер.
Жировая ткань и прежде всего ее забрюшинная часть секретирует большое количество биологически активных веществ, что позволяет ряду исследователей рассматривать ее как самостоятельный компонент эндокринной системы [27, 28]. Многие из этих веществ играют важную роль в развитии ИР, однако они также могут приводить к возникновению гипогонадизма. В частности, лептин, секреция которого жировой тканью при МС повышена, способен непосредственно подавлять чувствительность клеток Лейдига к лютеинизирующему гормону в результате взаимодействия со специфическими рецепторами [29].
Другой механизм связи между жировой тканью и тестостероном известен уже довольно давно и заключается в превращении андрогенов в эстрогены в жировых клетках в результате действия фермента ароматазы [30]. Таким образом, жировая ткань способна не только подавлять секрецию тестостерона, но и снижать его активность, повышая при этом концентрацию его естественных антагонистов.
Таким образом, жировая ткань способна не только подавлять секрецию тестостерона, но и снижать его активность, повышая при этом концентрацию его естественных антагонистов.
Предполагается, впрочем, и существование обратного эффекта. В ряде экспериментальных работ показано, что тестостерон стимулирует липолиз в жировых клетках [28], угнетает поступление в них липидных молекул из крови [31], а также подавляет дифференцировку стволовых клеток в адипоциты [32]. Все эти данные указывают на то, что уровень тестостерона в крови влияет на жировую ткань. Подтверждением обоснованности предположений такого рода являются результаты клинических исследований, показавших возможность уменьшения объема жировой ткани у мужчин на фоне лечения препаратами тестостерона, о которых речь пойдет ниже.
На основании представленных выше данных о связи между жировой тканью и тестостероном предложено несколько теорий, объясняющих развитие гипогонадизма у больных с ожирением (и наоборот). Согласно одной из подобных теорий [33], жировые клетки превращают тестостерон в эстроген, а также синтезируют вещества, подавляющие функцию клеток Лейдига, приводя к развитию гипогонадизма. Это в свою очередь подавляет липолиз и стимулирует захват жировыми клетками липидов из крови, что ведет к увеличению объема жировой ткани и дальнейшему усилению метаболизма тестостерона. При этом вследствие повышенного уровня эстрогенов и адипоцитокинов угнетается гипоталамо-гипофи-зарная реакция на снижение концентрации тестостерона. Подобная гипотеза, в частности, объясняет тот факт, что у мужчин с ожирением и гипогонадизмом не отмечается компенсаторного повышения уровня лютеинизи-рующего и фолликуло-стимулирующего гормонов.
Согласно одной из подобных теорий [33], жировые клетки превращают тестостерон в эстроген, а также синтезируют вещества, подавляющие функцию клеток Лейдига, приводя к развитию гипогонадизма. Это в свою очередь подавляет липолиз и стимулирует захват жировыми клетками липидов из крови, что ведет к увеличению объема жировой ткани и дальнейшему усилению метаболизма тестостерона. При этом вследствие повышенного уровня эстрогенов и адипоцитокинов угнетается гипоталамо-гипофи-зарная реакция на снижение концентрации тестостерона. Подобная гипотеза, в частности, объясняет тот факт, что у мужчин с ожирением и гипогонадизмом не отмечается компенсаторного повышения уровня лютеинизи-рующего и фолликуло-стимулирующего гормонов.
Нарушения липидного обмена, проявляющиеся в форме атерогенной дислипидемии, также коррелируют с уровнем тестостерона в крови. При этом мужчины с гипогонадизмом имеют склонность к повышению уровня общего холестерина (ХС) и ХС липопротеидов низкой плотности (ЛПНП) [34, 35], в то время как концентрация ХС липопротеидов высокой плотности (ЛПВП) в этой группе понижена [36]. Эти нарушения могут быть скорректированы путем применения препаратов тестостерона. Показана также связь снижения концентрации тестостерона в крови и артериальной гипертензии [37].
Эти нарушения могут быть скорректированы путем применения препаратов тестостерона. Показана также связь снижения концентрации тестостерона в крови и артериальной гипертензии [37].
Ведущим механизмом развития ССЗ является эндотелиальная дисфункция. Все описанные выше сосудистые факторы риска оказывают негативное действие на функциональное состояние эндотелия, что ведет к развитию атеросклероза и его осложнений. В то же время гипогонадизм может непосредственно вызывать повреждение эндотелия. В эксперименте на крысах YL. Lu в! а1. обнаружили, что кастрация и введение антагонистов 5-а-редуктазы, нарушающих превращение тестостерона в его биологически активную форму дигидротестостерон, сопровождаются выраженными изменениями в эндотелиальных клетках [38]. При микроскопическом исследовании эндотелиальные клетки были сморщенными, их форма — измененной, а межклеточные соединения — нарушенными. Кроме того, многие эндотелиальные клетки были покрыты эритроцитами. В группе кастрированных животных эти изменения были более выраженными, и они частично подвергались обратному развитию в результате введения тестостерона.
Предполагается также, что тестостерон и другие андрогены стимулируют пролиферацию в костном мозге предшественников эндотелиальных клеток, а также их выход в кровоток и соединение с областями дефектов эндотелия. У молодых мужчин с гипогонадизмом отмечено снижение концентрации предшественников эндотелиальных клеток в крови, при этом заместительная терапия приводила к существенному росту этих показателей [39]. Кроме того, биологически активная форма тестостерона — дигидротестостерон также стимулирует пролиферацию самих эндотелиальных клеток сосудов. Подобный эффект дигидротестостерона показан в экспериментах с использованием аорты быка [40] и сосудов человека [41].
Тестостерон также влияет на выделение эндотелиальными клетками различных пара- и аутокринных медиаторов, а также цитокинов. В частности, показано, что гипогонадизм сопровождается повышением уровня эн-дотелина-1, обладающего выраженным вазоконстрик-торным действием [42]. Лечение препаратами тестостерона сопровождалось снижением концентрации данного вещества.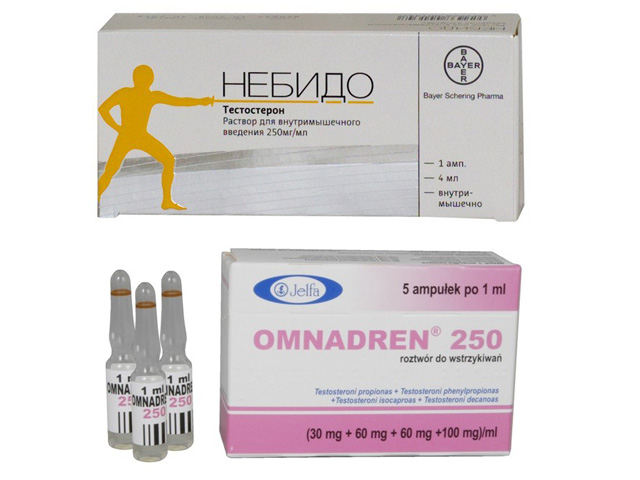 Тестостерон также подавляет синтез в эндотелии многих цитокинов [43], оказывающих негативное действие на функцию этих клеток.
Тестостерон также подавляет синтез в эндотелии многих цитокинов [43], оказывающих негативное действие на функцию этих клеток.
Пролиферация гладкомышечных клеток сосудов является важным этапом развития атеросклероза. На этот процесс также оказывает влияние уровень андрогенов в крови. Тестостерон и дигидротестостерон обладают ан-типролиферативным, проапоптическим действием в отношении гладкомышечных клеток сосудов [44, 45], что может давать антиатерогенный эффект.
Представленные выше данные о влиянии уровня андрогенов на развитие МС указывают на то, что наряду с прямым действием на эндотелий тестостерон также может оказывать свое влияние опосредованно через развитие различных сосудистых нарушений. Основным практическим следствием этого является теоретическая возможность устранения сосудистых факторов риска и, соответственно, предотвращения или замедления развития сердечно-сосудистых нарушений путем коррекции сниженного уровня тестостерона. Подобного эффекта можно достичь путем применения препаратов тестостерона.
Длительное время не существовало удобных в применении и эффективных препаратов тестостерона, однако на данный момент стал доступным ряд новых, высокоэффективных средств, значительно расширивших возможности коррекции уровня тестостерона. Среди этих средств есть различные формы препаратов, включая пероральные (применяются ограниченно), для в/м введения, накожного применения, а также имплантируемые гранулы, содержащие тестостерон.
Широкое применение в современной клинической практике получили препараты тестостерона для в/м введения. В большинстве случаев они позволяют достичь максимальной концентрации тестостерона в плазме крови в течение 72 ч после введения. В течение последующих 10–21 сут уровень тестостерона прогрессивно снижается. Наиболее часто применяют масляные растворы тестостерона энантата и ципионата, которые вводят в дозах от 200 до 400 мг каждые 3–4 нед. [46]. Существенным недостатком подобных препаратов является наличие при их применении значительных колебаний уровня тестостерона в крови.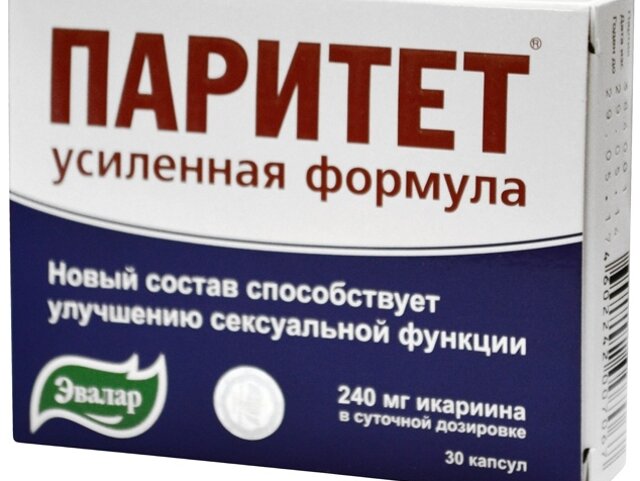 При этом в первые дни после введения уровень тестостерона часто значительно превышает физиологические значения, а в последние — уступает им.
При этом в первые дни после введения уровень тестостерона часто значительно превышает физиологические значения, а в последние — уступает им.
С целью преодоления этих недостатков, а также для достижения более удобного режима назначения был создан тестостерона ундеканоат для в/м введения. Данный препарат имеет уникальные фармакокинетические характеристики — при его применении стабильный уровень тестостерона в пределах физиологических значений достигается в течение 3 сут после введения и сохраняется около 12 нед. [47]. В связи с этим интервал между в/м инъекциями тестостерона ундеканоата (10–14 нед. или 4 р./год) почти в 5 раз превышает таковой для тестостерона энантата или ципионата (2–3 нед. или 17–26 инъекций/год). Эта особенность делает данный препарат более удобным для проведения длительной заместительной терапии.
Одна ампула препарата содержит 1000 мг тестостерона ундеканоата в 4 мл касторового масла. Содержимое ампулы следует вводить очень медленно (в течение примерно 60 с) глубоко в ягодичную область. После введения тестостерона ундеканоат постепенно выделяется в кровь, где он расщепляется эстеразами сыворотки с образованием тестостерона. Интервал между 1-й и 2-й инъекциями должен составлять 6 нед., между последующими — 12 нед. При применении тестостерона ундеканоата рекомендуется измерять уровень тестостерона в плазме 1 р./год.
После введения тестостерона ундеканоат постепенно выделяется в кровь, где он расщепляется эстеразами сыворотки с образованием тестостерона. Интервал между 1-й и 2-й инъекциями должен составлять 6 нед., между последующими — 12 нед. При применении тестостерона ундеканоата рекомендуется измерять уровень тестостерона в плазме 1 р./год.
Среди препаратов тестостерона для накожного применения выделяют пластыри и гели. Первые пластыри, содержащие тестостерон, были предложены в начале 1990-х гг. и предназначались для аппликации на кожу мошонки. Помимо неудобств, связанных с фиксацией, применение подобных пластырей сопровождается повышенным уровнем дигидротестостерона в крови, что объясняется восстановлением вводимого тестостерона 5-а-редуктазой, содержащейся в коже мошонки [48]. Этого недостатка лишены пластыри для применения вне мошонки, однако они часто (~32% случаев) вызывают раздражение кожи, а у 12% пациентов развивается аллергический дерматит [49]. Содержащие тестостерон гели реже вызывают раздражение кожи и позволяют добиться адекватного уровня гормона в крови. Предложена также форма для аппликации на слизистую щеки.
Предложена также форма для аппликации на слизистую щеки.
В настоящее время продолжается разработка препаратов тестостерона, имплантируемых подкожно в форме гранул и микрокапсул [50]. Эти препараты отличаются значительной длительностью действия (до 6 мес.), но имеют и существенные недостатки, основным из которых является необходимость проведения хирургических вмешательств при установке и удалении.
Тестостерон-заместительная терапия, как и любая другая форма лечения, сопряжена с риском развития побочных эффектов и осложнений, определяющих противопоказания к назначению препаратов тестостерона, а также объем наблюдения за пациентами в период подобного лечения. Традиционным опасением, связанным с применением препаратов тестостерона, является возможность повышения риска развития и/или прогрессирования РПЖ. В этой связи до начала, а также периодически в период проведения заместительной терапии необходимо выполнять пальцевое ректальное исследование и исследование уровня простатического специфического антигена в крови. Необходимо отметить, что накапливается все больше данных о том, что нормализация уровня тестостерона не сопровождается сколь-нибудь заметным негативным действием на течение РПЖ [51]. Кроме того, всем мужчинам до начала лечения, а также каждые 3 мес. в течение 1-го года терапии и ежегодно в дальнейшем необходимо проводить исследование уровня гематокрита. Это связано с тем, что тестостерон стимулирует эритропоэз, и у части больных значительное увеличение количества эритроцитов может сопровождаться опасным повышением вязкости крови.
Необходимо отметить, что накапливается все больше данных о том, что нормализация уровня тестостерона не сопровождается сколь-нибудь заметным негативным действием на течение РПЖ [51]. Кроме того, всем мужчинам до начала лечения, а также каждые 3 мес. в течение 1-го года терапии и ежегодно в дальнейшем необходимо проводить исследование уровня гематокрита. Это связано с тем, что тестостерон стимулирует эритропоэз, и у части больных значительное увеличение количества эритроцитов может сопровождаться опасным повышением вязкости крови.
Следует отметить, что одним из исторически бытовавших предубеждений, ограничивавших применение препаратов тестостерона, являлись опасения возможного негативного влияния на ССС. Однако, как мы уже указывали выше, лучшее понимание истинной природы взаимосвязи между уровнем тестостерона в крови и сосудистыми факторами риска создало предпосылки к изучению возможности коррекции последних в результате заместительной терапии препаратами тестостерона.
В литературе широко представлены результаты исследований влияния препаратов тестостерона на различные элементы МС [21, 52–64]. Наиболее подробно изучено действие препаратов тестостерона на избыточную жировую ткань. В целом ряде исследований показано, что гормонозаместительная терапия ведет к увеличению мышечной и уменьшению жировой массы. Следует отметить, что уменьшение жировой массы происходит в значительной мере за счет наиболее важной, с клинической точки зрения, абдоминальной ее части [54].
Так, в дважды слепом рандомизированном исследовании, проведенном PJ. Snyder et al., 108 мужчин в возрасте старше 65 лет, страдавших гипогонадизмом, получали лечение препаратом тестостерона или плацебо в течение 36 мес. [55]. По окончании исследования в группе, получавшей тестостерон, было отмечено снижение массы жировой ткани в среднем на 3 кг и повышение безжировой массы тела на 1,9 кг. Среди принимавших плацебо достоверных изменений отмечено не было. Возможность снижения выраженности или предотвращения развития ожирения и других компонентов МС в результате введения экзогенного тестостерона подтверждена и в исследованиях на животных [65].
Применение препаратов тестостерона может также приводить к нормализации уровня АД. Возможность подобного действия показана в исследованиях у мужчин, страдающих ожирением и СД 2-го типа [60, 66]. При этом отмечено, что восстановление нормального уровня тестостерона в крови в результате заместительной
терапии у больных с ИР сопровождается нормализацией уровня глюкозы в крови [60].
Влияние лечения препаратами тестостерона на липидный статус является неоднозначным. Было показано, что подобное лечение может приводить к снижению концентрации ХС ЛПВП — потенциально неблагоприятному эффекту. В то же время анализ различных фракций этой формы липопротеидов показал, что применение тестостерона преимущественно снижает концентрацию 3с формы, имеющей наименьшее значение для антиатерогенных свойств данного типа липопротеидов [67, 68]. При этом уровни других фракций, являющихся значительно более важными, даже повышались.
Между тем концентрация ХС ЛПНП, обладающего выраженной атерогенной активностью, на фоне лечения тестостероном, по данным большинства проведенных исследований, снижалась. Также было отмечено снижение и уровня общего ХС.
Также было отмечено снижение и уровня общего ХС.
В исследовании М. Zitzmann et al. было изучено влияние лечения тестостероном на уровень липидов в крови, а также АД у 66 мужчин с гипогонадизмом [69]. Проведенное лечение привело к достоверному снижению уровня ЛПНП, а также систолического и диастолического АД. В то же время концентрация ХС ЛПВП за период лечения выросла.
Выше мы указывали, что гипогонадизм способен оказывать негативное влияние на эндотелий, приводя к развитию эндотелиальной дисфункции. Последняя, наряду с гипогонадизмом, является ведущим патогенетическим механизмом развития эректильной дисфункции и сердечно-сосудистых осложнений у мужчин, страдающих МС. Эти сведения в сочетании с приведенными выше данными о благоприятных эффектах применения препаратов тестостерона на ССС указывают на то, что подобное лечение может также корректировать эндотелиальную дисфункцию.
Данный вопрос к настоящему времени изучен недостаточно подробно, однако есть отдельные сведения, позволяющие предполагать, что обсуждаемые эффекты, действительно, имеют место. В частности, продемонстрировано благоприятное действие лечения препаратами тестостерона на отдельные нарушения, играющие важную роль в развитии эндотелиальной дисфункции. Фармакотерапия, приводившая к нормализации уровня тестостерона в крови, сопровождалась снижением концентраций провоспалительных цитокинов [70] и эндотелина-1 [42], а также повышением концентрации эндотелиальных клеток-предшественников [71]. Эти результаты являются весьма многообещающими, и данный вопрос нуждается в дальнейшем изучении.
В частности, продемонстрировано благоприятное действие лечения препаратами тестостерона на отдельные нарушения, играющие важную роль в развитии эндотелиальной дисфункции. Фармакотерапия, приводившая к нормализации уровня тестостерона в крови, сопровождалась снижением концентраций провоспалительных цитокинов [70] и эндотелина-1 [42], а также повышением концентрации эндотелиальных клеток-предшественников [71]. Эти результаты являются весьма многообещающими, и данный вопрос нуждается в дальнейшем изучении.
Препараты тестостерона способны оказывать и непосредственное благоприятное действие на ССС. В частности, показано, что тестостерон вызывает расширение коронарных артерий. Подобный эффект продемонстрирован как в экспериментальных [72], так и в клинических [73] условиях. Предполагается, что это связано с активацией калиевых каналов. Возможное клиническое значение этих данных продемонстрировано в рандомизированном дважды слепом исследовании действия тестостерона на результаты теста с физической нагрузкой у мужчин со стабильной стенокардией напряжения [8]. В группе, получавшей тестостерон, отмечено повышение переносимости физической нагрузки, которое оценивали по изменениям электрокардиограммы. Степень улучшения была большей у пациентов, исходно имевших более тяжелые гормональные нарушения. Существование подобного эффекта подтверждено и в ряде других работ [8, 74–79]. Интересно, что впервые благоприятное действие тестостерона на стенокардию напряжения было описано более 60 лет назад [74].
В группе, получавшей тестостерон, отмечено повышение переносимости физической нагрузки, которое оценивали по изменениям электрокардиограммы. Степень улучшения была большей у пациентов, исходно имевших более тяжелые гормональные нарушения. Существование подобного эффекта подтверждено и в ряде других работ [8, 74–79]. Интересно, что впервые благоприятное действие тестостерона на стенокардию напряжения было описано более 60 лет назад [74].
Таким образом, гипогонадизм является важным патогенетическим элементом развития МС и ССЗ у мужчин. Связь между снижением уровня тестостерона и сосудистыми факторами риска, прежде всего ожирением и ИР, является двунаправленной, т. е. обе группы нарушений взаимно усугубляют друг друга, формируя порочный круг. Одним из перспективных способов коррекции подобных нарушений является использование препаратов тестостерона, доступных в настоящее время в удобной для клинического применения форме. Все эти препараты оказывают свое действие одинаковым способом и содержат одно и то же действующее вещество, однако пути его доставки в системный кровоток и через него к тканям и органам различны. Выбирая наиболее подходящий для каждого конкретного случая препарат, следует учитывать многие факторы, включая индивидуальные предпочтения пациента.
Выбирая наиболее подходящий для каждого конкретного случая препарат, следует учитывать многие факторы, включая индивидуальные предпочтения пациента.
Побочные эффекты терапии тестостероном | Риск сердечного приступа и рака
Фармацевтические компании, производящие препараты для замены тестостерона, такие как AndroGel, интенсивно продвигают свою продукцию, обещая мужчинам увеличение жизненной силы, силы, полового влечения и общее улучшение качества жизни.
Реальность, однако, такова, что заместительная терапия тестостероном (ЗТТ) может вызвать ряд осложнений со здоровьем, которые, по мнению некоторых врачей, не стоят пользы.
Исследования и клинические испытания связывают лекарства с серьезными рисками для здоровья, включая проблемы с сердцем и рак. Заместительная терапия также может нарушить баланс гормонов в организме. Яички могут уменьшиться, и существует риск необратимого бесплодия. Женщины, дети и домашние животные также могут испытывать серьезные побочные эффекты при контакте с продуктами TRT.
Данные опубликованных исследований и мнение экспертов консультативного комитета побудили Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) потребовать изменения маркировки, чтобы отразить дополнительные риски, связанные с использованием этих продуктов. Тем не менее, критики, в том числе истцы в более чем 25 000 судебных процессов, говорят, что необходимо еще больше предупреждений о побочных эффектах.
Серьезные побочные эффекты возникают редко, а побочные эффекты, о которых чаще всего сообщалось в клинических испытаниях, были в основном незначительными. Наиболее часто сообщаемые нежелательные явления в клинических испытаниях варьировались в зависимости от продукта, но, как правило, они включали реакции в месте нанесения, увеличение мужской груди, жирную кожу и изменения в структуре и росте волос. Другие зарегистрированные побочные эффекты включали акне, заболевания предстательной железы, боли в спине и аномальные лабораторные анализы.
Риск сердечного приступа
Результаты клинического исследования, опубликованные в Журнале Американской медицинской ассоциации (JAMA) в феврале 2017 года, показали, что лечение пожилых мужчин гелем тестостерона в течение одного года было связано со значительным увеличением бляшек в коронарных артериях. Воскообразное вещество может накапливаться, затвердевать и уменьшать приток кислорода к сердцу. Если артерия полностью блокируется, это может привести к сердечному приступу, также известному как инфаркт миокарда.
Исследование, которое должно завершиться в конце 2022 года под названием «Заместительная терапия тестостероном для оценки долгосрочных сосудистых событий и эффективности реакции у мужчин с гипогонадизмом» (TRAVERSE). Исследование обещает собрать больше данных о терапии тестостероном и сердечном риске. По состоянию на 2 декабря 2022 г. результаты не опубликованы.
«Лечение [Т]эстостероном по сравнению с плацебо было связано со значительно большим увеличением объема некальцифицированных бляшек по сравнению с исходным уровнем до 12 месяцев».
Исследователи в течение года изучали влияние лечения на здоровье сердечно-сосудистой системы у мужчин с низким уровнем тестостерона, который нельзя было объяснить ничем, кроме возраста. Всего исследование завершили 138 мужчин старше 64 лет; 73 человека получили препараты, а 65 — плацебо.
«Лечение [Т]эстостероном по сравнению с плацебо было связано со значительно большим увеличением объема некальцифицированных бляшек по сравнению с исходным уровнем до 12 месяцев», — пишут авторы исследования. Они отметили, что для оценки риска необходимы дополнительные, более масштабные исследования.
Исследование, опубликованное в 2014 году в журнале PLOS One, показало, что риск сердечного приступа после начала ЗТТ «значительно повышается» у пожилых мужчин и у молодых мужчин с ранее диагностированным заболеванием сердца.
Исследование, проведенное Уильямом Д. Финклем и его коллегами, включало записи 55 000 мужчин, которым прописали тестостерон в США. Было обнаружено, что в первые 9Через 0 дней после начала терапии риск сердечного приступа у мужчин в возрасте 65 лет и старше, принимавших наркотики, удваивался по сравнению с теми, кто не принимал наркотики в той же возрастной группе.
Риск не ограничивался пожилыми мужчинами. Исследование также показало, что мужчины моложе 65 лет с ранее существовавшим заболеванием сердца имели в два-три раза повышенный риск сердечного приступа в течение 90 дней после начала терапии.
Авторы исследования отметили, что их результаты согласуются с анализом плацебо-контролируемых рандомизированных исследований, в которых сообщалось, что ЗТТ увеличивает риск сердечного приступа и других серьезных сердечно-сосудистых рисков. В испытаниях участвовали в основном пожилые мужчины, которые принимали наркотики в течение 12 и более недель.
«В совокупности данные подтверждают связь между терапией тестостероном и риском серьезных, неблагоприятных сердечно-сосудистых событий, включая несмертельный инфаркт миокарда, у мужчин», — написали Финкл и его коллеги.
Кроме того, исследование, опубликованное в JAMA в ноябре 2013 года, показало 30-процентное повышение риска сердечных приступов и других сердечно-сосудистых заболеваний у ветеранов, принимавших заместительную гормональную терапию, по сравнению с теми, кто этого не делал, по данным FDA.
Исследование остановлено из-за «значительно более высокой» частоты сердечно-сосудистых событий
Исследователи остановили небольшое исследование в 2010 году, поскольку частота неблагоприятных сердечно-сосудистых событий была значительно выше в группе, принимавшей тестостерон, чем в группе, не принимавшей препараты.
Медицинский журнал Новой Англии опубликовал результаты исследования, в котором участвовали ослабленные пожилые мужчины, принимавшие ЗТТ. В общей сложности 23 мужчины в группе, принимавшей препараты, страдали сердечно-сосудистыми побочными эффектами по сравнению с пятью мужчинами в группе плацебо.
«Совет по мониторингу данных и безопасности рекомендовал прекратить исследование досрочно, потому что частота неблагоприятных сердечно-сосудистых событий в группе тестостерона была значительно выше, чем в группе плацебо», — пишут авторы исследования.
Призывы к предупреждению в черном ящике
Риск сердечно-сосудистых заболеваний побудил группы защиты прав потребителей призывать к предупреждению в черном ящике на всех упаковках препаратов тестостерона. Доктор Сидни Вулф из Public Citizen заявил в подкасте Drugwatch 2014 года, что организация обратилась в FDA с ходатайством потребовать от производителей добавлять предупреждения на упаковки нескольких продуктов для замены гормонов, уже находящихся на рынке.
Доктор Сидни Вулф из Public Citizen заявил в подкасте Drugwatch 2014 года, что организация обратилась в FDA с ходатайством потребовать от производителей добавлять предупреждения на упаковки нескольких продуктов для замены гормонов, уже находящихся на рынке.
Предыдущие исследования «показали, что риск сердечно-сосудистых заболеваний увеличился на 50 процентов… 14 исследований, которые не финансировались фармацевтической промышленностью, [показали] более чем удвоение рисков», — сказал Вулф в интервью Drugwatch.
«[Предыдущие исследования] показали 50-процентное увеличение сердечно-сосудистого риска. . . 14 исследований, которые не финансировались фармацевтической промышленностью, [показали] более чем удвоение рисков».
Финкл повторил мнение Вулфа в интервью NPR в 2014 году.
«У нас есть исследование 2010 года, которое было отменено из-за неожиданного сердечно-сосудистого риска», — сказал Финкл NPR. «Я думаю, этого было достаточно, чтобы оправдать предупреждение. Зачем скрывать это от пациента?»
Зачем скрывать это от пациента?»
До настоящего времени FDA не требовало предупреждения о риске сердечно-сосудистых заболеваний в виде «черного ящика», но в 2015 году агентство потребовало от производителей препаратов ЗТТ добавлять на этикетки продуктов информацию о возможном повышенном риске сердечных приступов.
Предупреждение о тромбах
В июне 2014 г. FDA потребовало от производителей ТЗТ размещать на этикетках лекарств предупреждение о риске образования тромбов в венах. На этикетках теперь говорится, что были постмаркетинговые отчеты о том, что использование этих продуктов привело к серьезным тромбам.
Тестостерон увеличивает выработку тромбоксана, липида, который способствует сужению кровеносных сосудов. Это может замедлить кровоток, повышая вероятность образования тромбов. Тромбоз глубоких вен возникает, когда эти сгустки образуются в крупных венах, обычно в ногах. Если эти сгустки вырвутся на свободу, они могут попасть в легкие и вызвать легочную эмболию или попасть в мозг и вызвать инсульт.
Сгустки крови, образующиеся внутри вен и не растворяющиеся естественным образом, очень опасны и могут привести к летальному исходу.
Другим побочным эффектом ЗТТ является полицитемия, состояние, характеризующееся повышенным уровнем эритроцитов. Когда костный мозг вырабатывает слишком много эритроцитов, это приводит к сгущению крови и увеличивает риск образования тромбов.
Исследование показало, что тромбы образуются уже через 3 недели после начала терапии
Исследование, впервые опубликованное 7 августа 2013 г. в журнале Clinical and Applied Thrombosis/Hemostasis, показало, что тромбы образуются уже через три недели после начала терапии тестостероном у мужчин. наркотики.
Исследование выявило семь мужчин, которые принимали наркотики до или во время госпитализации по поводу серьезных тромбов. У мужчин образовались тромбы через 3 недели, 1 месяц, 2 месяца, 3 месяца, 12 месяцев или 27 месяцев после начала ЗТТ.
«Наше исследование показало, что у 1,2% мужчин, попавших в больницу с опасными и потенциально смертельными тромбами в глубоких венах ног или в легких, эти тромбы развились в течение трех месяцев после начала терапии тестостероном», — говорит автор исследования д-р. Об этом Cincinnati Business Courier сообщил Чарльз Глюк из Центра холестерина и метаболизма Еврейской больницы.
По словам Глюка, наследственное нарушение свертываемости крови может увеличить риск образования тромбов. Он сказал, что люди должны быть проверены на факторы риска перед началом ЗТТ.
Потенциальный риск инсульта
В марте 2015 года FDA потребовало от производителей обновить этикетки своих продуктов, чтобы предупредить о возможном повышенном риске инсульта у пациентов, принимающих тестостерон. По данным FDA, некоторые исследования показали повышенный риск инсульта, связанного с ЗТТ, но результаты исследований неоднозначны.
«Некоторые постмаркетинговые исследования показали повышенный риск [сердечного приступа] и инсульта, связанный с использованием заместительной терапии тестостероном», — говорится на этикетке Testim, одобренной FDA.
«Некоторые постмаркетинговые исследования показали повышенный риск [сердечного приступа] и инсульта, связанный с использованием заместительной терапии тестостероном».
Исследование 2010 года, опубликованное в Медицинском журнале Новой Англии, показало, что препараты могут повышать риск нескольких сердечно-сосудистых заболеваний, включая инсульт у пожилых мужчин с ограниченной подвижностью и высокой распространенностью хронических заболеваний. Но Шехзад Басари и другие авторы предупредили, что размер исследования небольшой — всего 209мужчины 65 лет и старше — потребовали дальнейшего изучения рисков.
В исследовании, проведенном в июле 2015 года в журнале JAMA Internal Medicine, сравнивались различные системы доставки препаратов ЗЗТ. Было обнаружено, что инъекции были связаны с повышенным краткосрочным риском инсульта и других осложнений. Риск был ниже при использовании гелей и пластырей.
Более поздние исследования поставили под сомнение степень риска инсульта при использовании ЗТТ.
В исследовании, опубликованном в сентябре 2017 года в журнале Maturitas, были рассмотрены предыдущие исследования взаимосвязи между этими лекарствами и риском инсульта. Выяснилось, что несколько исследований специально рассматривали риск инсульта у мужчин, получавших тестостерон, а исследования, в которых оценивалась возможная связь, имели серьезные ограничения. Исследователь Симона Лу и другие авторы пришли к выводу, что «связь между ЗТТ и риском инсульта у мужчин остается неясной».
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов заявило, что требует от производителей проведения клинических испытаний, чтобы определить, существует ли повышенный риск инсульта среди пользователей тестостерона. Агентство поручило медицинским работникам предупреждать пациентов о потенциальном риске, а также предупредило пациентов, принимающих препараты ЗТТ, немедленно обратиться за медицинской помощью, если у них появятся симптомы инсульта, включая невнятную речь и слабость в одной части или одной стороне тела.
Препараты ЗТТ также связаны с возможным увеличением риска развития рака предстательной железы. Одной из причин этого является всплеск уровня тестостерона.
Исследования, связывающие препараты ЗТТ с риском развития рака предстательной железы, восходят к рубежу веков.
Одно исследование под руководством доктора Терренса Шейнифелта обнаружило двукратное увеличение риска рака простаты среди мужчин, у которых уровень тестостерона находился в самой высокой квартиле. Авторы исследования были из Медицинского центра Beth Israel Deaconess и Гарварда.
В исследовании 2005 года, опубликованном в Journal of Urology, были рассмотрены медицинские записи шести урологических клиник. Они рассмотрели случаи, когда мужчины проходили терапию по поводу сексуальной дисфункции или «омоложения», и выявили 20 мужчин, у которых был диагностирован рак простаты после начала ЗТТ.
В 55 процентах случаев врачи обнаруживали рак в течение двух лет после того, как мужчины впервые начали употреблять наркотики. У остальных мужчин диагноз был поставлен в период от 28 месяцев до 8 лет после начала терапии.
У остальных мужчин диагноз был поставлен в период от 28 месяцев до 8 лет после начала терапии.
«Рак предстательной железы может стать клинически очевидным в течение нескольких месяцев или нескольких лет после начала лечения тестостероном».
«Рак предстательной железы может стать клинически очевидным в течение нескольких месяцев или нескольких лет после начала лечения тестостероном», — заключили авторы. «Врачи, назначающие добавки с тестостероном, и пациенты, получающие их, должны осознавать этот риск, и во время лечения следует часто проводить тест на уровень ПСА в сыворотке и пальцевое ректальное исследование».
Но почти через два десятилетия после завершения первого из этих исследований исследователи говорят, что необходимы дополнительные исследования.
В 2017 году Национальные институты здравоохранения завершили широкомасштабное исследование ЗТТ под названием «Испытания тестостерона» (Тиспытания). Проект координировал семь плацебо-контролируемых двойных слепых испытаний — золотой стандарт медицинских исследований. Выводы относительно точной связи между терапией и раком предстательной железы были неубедительными.
Выводы относительно точной связи между терапией и раком предстательной железы были неубедительными.
«Хотя тестостерон не был связан с большим количеством побочных эффектов со стороны сердечно-сосудистой системы или простаты, чем плацебо, необходимо провести исследование с гораздо большим числом мужчин в течение гораздо более длительного периода, чтобы определить, увеличивает ли тестостерон риск сердечно-сосудистых заболеваний или простаты», — пишут исследователи.
Тем временем FDA требует, чтобы этикетки продуктов рекомендовали врачам контролировать мужчин, принимающих терапию, чтобы убедиться, что рак простаты не развивается. Мужчины, у которых есть проблемы с простатой, не должны использовать продукты.
Исследования на животных
Исследование, проведенное в 2014 году под руководством профессора Маартена Босланда из Университета Иллинойса в Чикагском медицинском колледже, показало, что у крыс, подвергшихся воздействию известного канцерогена, не развился рак, но у 10–18 процентов крыс, подвергшихся воздействию тестостерон сделал.
Кроме того, от 50 до 71 процента крыс, подвергшихся воздействию как канцерогена, так и гормона, заболели раком простаты. Согласно исследованию, даже низких доз препарата для замены гормонов было достаточно для образования опухолей.
«Если эти же результаты верны для людей, есть серьезная причина для беспокойства общественного здравоохранения», — сказал Босланд в статье UIC Today.
Апноэ во сне может ухудшиться
Заместительная терапия тестостероном может усугубить апноэ во сне или увеличить вероятность его развития, особенно у пациентов с такими факторами риска, как ожирение или хронические заболевания легких, согласно этикеткам препаратов.
Некоторые исследователи обнаружили, что ЗТТ может усугубить тип апноэ во сне, известный как обструктивное апноэ во сне (СОАС), но другие говорят, что связь между терапией и состоянием сна была слабой.
При ОАС поток воздуха прекращается или уменьшается во время сна из-за закупорки или сужения дыхательных путей. Это может вызвать инсульт, мерцательную аритмию и ишемию сердца, состояние, при котором к сердцу поступает недостаточно крови.
Это может вызвать инсульт, мерцательную аритмию и ишемию сердца, состояние, при котором к сердцу поступает недостаточно крови.
«Заслуживает внимания повышенный риск СОАС у мужчин, принимающих ЗТТ».
В статье, опубликованной в 2007 году в «Журнале сексуальной медицины», говорится, что необходимы дальнейшие исследования, чтобы определить, существует ли связь между гормональной терапией и синдромом обструктивного апноэ во сне. Автор проанализировал литературу о ЗТТ и СОАС и пришел к выводу, что «отсутствуют убедительные доказательства» того, что такое лечение вызывает или ухудшает состояние сна. Автор отметил, что в большинстве исследований участвовало небольшое количество мужчин.
В исследовании 2012 года, опубликованном в журнале Clinical Endocrinology, изучалась группа из 67 мужчин с ожирением, страдающих тяжелым синдромом обструктивного апноэ во сне. В ходе рандомизированного двойного слепого плацебо-контролируемого исследования всем участникам была назначена низкокалорийная диета, а затем мужчинам вводили либо гормон, либо плацебо в течение 12 недель.
«Терапия тестостероном у тучных мужчин с тяжелой формой ОАС незначительно ухудшает нарушение дыхания во сне в течение ограниченного времени, независимо от начальных концентраций тестостерона», — написали Камилла Хойос и другие авторы.
Более свежее исследование, опубликованное в марте 2018 года в BJU International, показало, что риск СОАС был выше у мужчин, получавших тестостерон, чем у тех, кто не получал терапию. В исследовании приняли участие 3422 мужчины в возрасте от 40 до 64 лет, которым в период с 2006 по 2010 год была назначена ЗТТ для лечения низкого уровня гормона. Исследователи сопоставили этих мужчин по возрасту и истории болезни с участниками, которым не прописывали лекарства.
По результатам исследования двухлетний риск СОАС составил 16,5% в группе, получавшей препараты, по сравнению с 12,7% в контрольной группе.
«Заслуживает внимания повышенный риск СОАС у мужчин, принимающих ЗТТ», — пишут авторы.
Риски для женщин
FDA не одобрило применение ЗТТ у женщин. Тем не менее, некоторые врачи начали добавлять тестостерон у женщин, как правило, в рамках режима заместительной гормональной терапии в среднем возрасте, чтобы противостоять симптомам перименопаузы и менопаузы.
Тем не менее, некоторые врачи начали добавлять тестостерон у женщин, как правило, в рамках режима заместительной гормональной терапии в среднем возрасте, чтобы противостоять симптомам перименопаузы и менопаузы.
Женщины, которым назначена ЗТТ или которые случайно контактируют с продуктами, должны знать о возможных побочных эффектах.
Возможные побочные эффекты для женщин включают:
- Рост волос на лице или теле
- Выпадение волос на коже головы
- Жирная кожа или прыщи
- Охриплость или огрубение голоса
- Задержка жидкости
- Уменьшенный размер груди
- Увеличенный размер клитора
Исследователи пока не знают, могут ли эти препараты влиять на такие факторы, как риск рака молочной железы, сердечных заболеваний или образования тромбов у женщин. Однако продукты этого класса имеют категорию X для беременных, что означает, что они могут нанести вред плоду.
Беременные женщины, которые могут забеременеть или кормящие грудью, не должны использовать тестостерон и должны избегать контакта с участками кожи, на которые были нанесены гели для местного применения. Нерожденные и грудные дети могут испытывать неадекватную вирилизацию, которая представляет собой развитие мужских вторичных половых признаков у женщин или очень раннее развитие таких признаков у мальчиков.
Предупреждение «черного ящика» о вторичном воздействии на детей
Случайное воздействие на детей, которые живут или общаются в тесном контакте с мужчинами, принимающими местные препараты тестостерона, представляет собой серьезную проблему. Это воздействие обычно происходит при контакте с кожей, обработанной гелями или другими продуктами для местного применения. По этой причине FDA требует, чтобы эти продукты содержали предупреждения на своих этикетках, чтобы информировать пользователей об опасности случайного воздействия и информировать пользователей о том, как этого избежать.
Два геля TRT, AndroGel и Testim, содержат предупреждение о вторичном воздействии на детей. Поскольку гель наносится на кожу, дети могут соприкасаться с местами нанесения или даже с остатками геля на нестиранной одежде или полотенцах.
Предупреждение в черном ящике гласит:
- Дети, подвергшиеся воздействию геля, могут страдать от неадекватной вирилизации.
- Дети не должны контактировать с «немытыми или раздетыми местами нанесения».
- Врачи и другие поставщики медицинских услуг должны предупреждать пациентов о том, что эти продукты следует использовать по назначению и строго следовать инструкциям по применению.
Побочные эффекты, зарегистрированные у детей, которые вступили в контакт с этими препаратами, включают увеличение гениталий, преждевременный рост лобковых волос, повышенную самостимуляцию и агрессивное поведение.
Хотя эти эффекты обычно исчезают после прекращения воздействия, в некоторых случаях гениталии могут оставаться увеличенными. Кроме того, у детей, подвергшихся воздействию этих препаратов, может наблюдаться преждевременное старение костей. В результате эти дети могут преждевременно перестать расти и во взрослом возрасте могут быть ниже ростом, чем могли бы быть без воздействия.
Кроме того, у детей, подвергшихся воздействию этих препаратов, может наблюдаться преждевременное старение костей. В результате эти дети могут преждевременно перестать расти и во взрослом возрасте могут быть ниже ростом, чем могли бы быть без воздействия.
Опасность для домашних животных
Существует мало исследований опасности, которую гели TRT могут представлять для домашних животных. На их этикетках просто упоминается, что пациенты должны «предотвращать случайное воздействие на детей или домашних животных», не подвергая животных особому риску.
Тем не менее, в 2010 году Ветеринарная информационная сеть, служба новостей для ветеринаров, подробно описала примерно 20 случаев побочных эффектов у домашних животных после контакта с гормональными пластырями или гелями. Большинство случаев касалось продуктов с эстрогеном, прописанных женщинам, но ветеринары поспешили включить предупреждения и о продуктах ЗТТ.
Служба Medline Plus Национального института здравоохранения сообщает, что домашние животные могут тереться об открытые участки кожи в местах нанесения препарата или играть с выброшенными конвертами или пластырями. Он рекомендует утилизировать использованные контейнеры или пластыри с препаратами TRT таким образом, чтобы защитить их от собак, кошек и других домашних животных.
Он рекомендует утилизировать использованные контейнеры или пластыри с препаратами TRT таким образом, чтобы защитить их от собак, кошек и других домашних животных.
Список лучших добавок тестостерона
Различные добавки и лекарства могут помочь повысить уровень тестостерона у человека. Однако повышение уровня тестостерона может повысить риск сердечно-сосудистых заболеваний, таких как сердечный приступ или инсульт.
Некоторые люди предпочитают повышать уровень тестостерона с помощью альтернативных методов лечения, хотя многие из них не имеют научной поддержки.
Обычно человек должен принимать добавки тестостерона только в том случае, если у него есть заболевание, вызывающее низкий уровень тестостерона. В качестве альтернативы они могут сделать это, если они трансгендеры и решат принимать добавки в рамках своего переходного процесса.
Согласно статье 2017 года, врачи обычно вводят тестостерон с помощью инъекций или трансдермально через кожу человека.
Узнайте больше о преимуществах и рисках приема тестостерона.
Человек может получать инъекции тестостерона у своего врача, или медицинский работник может позволить ему сделать себе инъекцию дома.
Эти инъекции обычно представляют собой энантат тестостерона или ципионат тестостерона, которые люди используют каждые 1–2 недели.
Однако эти инъекции могут повредить ткани, поэтому важно чередовать места инъекций и использовать стерильную технику.
Инъекции очень эффективны при лечении гипогонадизма и обеспечивают постоянство дозы, которую получает человек.
Трансдермальный тестостерон представляет собой гель, который люди наносят непосредственно на кожу. Этот метод лечения популярен, так как прост в применении.
Однако есть некоторые недостатки, такие как:
- возможное раздражение кожи
- гель может передаться другому человеку через контакт с кожей
- гель может стереться, уменьшая необходимую дозу
Если у человека есть проблемы с этими методами введения тестостерона, врач может предложить следующие альтернативы:
- подкожная таблетка тестостерона, которая находится под кожей
- введение тестостерона в нос или щеку
- прием тестостерона перорально
Они могут быть более удобными для человека, но они также могут увеличить вероятность раздражения или инфекции.
Чтобы выбрать правильный метод введения, люди должны проконсультироваться со своим врачом. Они также могут спросить о потенциальных затратах и преимуществах их конкретной истории болезни и их необходимости изучить подходящие альтернативы.
Сообщается, что многие добавки тестостерона, доступные без рецепта, повышают уровень тестостерона у человека. Однако, как правило, существует мало доказательств, подтверждающих их эффективность.
Изменения образа жизни, такие как физические упражнения, улучшение питания и поддержание умеренного веса, могут иметь более значительный эффект, чем прием этих добавок.
Человек должен рассмотреть эти варианты после обсуждения с врачом, который может помочь найти подходящий для него подход.
D-аспарагиновая кислота
Согласно исследованию 2017 года, D-аспарагиновая кислота повышает уровень тестостерона у некоторых животных. Однако исследования, изучающие его влияние на человека, неубедительны и в основном низкого качества. В документе говорится, что существует острая необходимость в дополнительных исследованиях этого химического вещества, которое естественным образом встречается в некоторых тканях человека.
В документе говорится, что существует острая необходимость в дополнительных исследованиях этого химического вещества, которое естественным образом встречается в некоторых тканях человека.
Дегидроэпиандростерон
Дегидроэпиандростерон (ДГЭА) — это гормон, который вырабатывается в организме, и люди могут приобрести его в качестве добавки к тестостерону. Однако статья 2016 года предполагает, что было мало доказательств его эффективности.
Травяные добавки
Согласно предыдущей статье в Американском журнале мужского здоровья , производители продают различные травяные добавки, которые, как сообщается, улучшают уровень тестостерона. Иногда они доступны в сочетании с DHEA.
Как и в случае с другими альтернативными вариантами лечения, существует мало доказательств их эффективности в повышении уровня тестостерона. Кроме того, могут возникнуть опасения по поводу дозировки, качества и чистоты этих продуктов, которые не подпадают под регулирующий надзор Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA).
Здесь мы отвечаем на некоторые распространенные вопросы об этих добавках.
Является ли чистый тестостерон стероидом?
Тестостерон — это гормон, вырабатываемый мужчинами в яичках. Женский организм также вырабатывает этот гормон в яичниках и надпочечниках, но в меньших количествах. Медицинские работники могут рекомендовать заместительную терапию тестостероном людям с гипогонадизмом.
Анаболические стероиды содержат натуральный или синтетический тестостерон. Однако анаболические стероиды не подходят в качестве замены заместительной терапии тестостероном.
Какой лучше принимать тестостерон?
Существуют различные способы приема тестостерона, например, подкожно, путем инъекции гормона или перорально.
Медицинский работник посоветует человеку, какой метод лучше всего подходит для его нужд.
Вы можете купить тестостерон?
Тестостерон можно приобрести только по действительному рецепту врача.
Однако люди никогда не должны покупать этот гормон на веб-сайтах или в других магазинах, где не требуется рецепт.
Нужно ли человеку принимать добавки тестостерона?
По мере взросления уровень тестостерона снижается, что может привести к следующему:
- снижение либидо
- эректильная дисфункция
- ослабление мышц и костей
противодействовать этим естественным эффектам старения. Однако возможная польза от приема тестостерона должна быть сбалансирована с более высоким риском сердечно-сосудистых заболеваний.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) не рекомендует принимать добавки тестостерона для противодействия эффектам старения из-за этих более высоких рисков.
Если человек совершает переход, он может выбрать терапию тестостероном, чтобы сделать аспекты своего тела, которые общество считает мужскими, более очевидными.
Согласно статье 2016 года, врач должен объяснить потенциальные риски гормональной терапии человеку, рассматривающему это лечение. Затем человек может принять лучшее решение о потенциальных выгодах, которые он может получить, и сопоставить их с рисками.