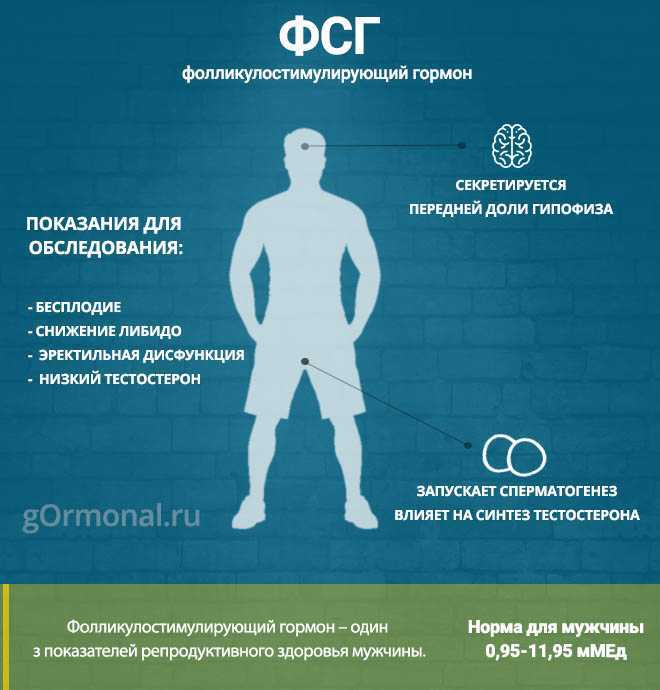
Повышенный и пониженный гормон ФСГ: лечение
Гормональный фон организма играет первостепенную роль в общем и репродуктивном здоровье женщины. В статье мы поговорим о фолликулостимулирующем и лютеинизирующем гормоне, норме их концентрации, возможных отклонениях и вариациях лечения подобного рода нарушений.
Гормоны ЛГ и ФСГ: за что они ответственны?
Гонадотропные гормоны, вырабатываемые в одноименной доле гипофиза, отвечают за продолжение рода. Таким образом, репродуктивное здоровье во многом обусловливается именно гормон ФСГ у женщин. Он вырабатывается также и у мужчин, отвечая за:
- рост семенников и семенных каналов;
- синтез и белковый обмен;
- сперматогенез.
У представительниц прекрасного пола данные гормоны регулируют:
- созревание яйцеклетки;
- рост фолликулов;
- синтез эстрогенов;
- трансформация тестостерона в эстрогены;
- ряд других функций.

В большинстве случаев, анализ ФСГ проводится при подозрении нарушения гормонального фона, что может стать причиной бесплодия. Кроме всего прочего, подобные обследования позволяют определить менструальный цикл, выявить причины нарушения сперматогенеза и половых дисфункций, а также провести диагностику раннего и позднего полового развития, осуществлять контроль проводимой гормонотерапии. Если по тем или иным причинам снижен или повышен уровень ФСГ, лечение выявленной патологии происходит комплексно.
Как проводится анализ крови на ФСГ и как подготовиться к его проведению?
Подобные анализы назначаются при бесплодии, половых дисфункциях, а также при подозрении на нарушение функции гипофиза и врожденных патологиях хромосомного характера. Следует сказать, что данный анализ в совокупности с другими обследованиями позволяет выявить первичные и вторичные гормональные нарушения. Таким образом, определение ФСГ и ЛГ носит аналитический и диагностический характер.
Для того, чтобы рассчитать соотношение ЛГ и ФСГ в конкретном случае, необходимо пройти одноименное исследование. Сдача биологического материала происходит примерно на пятый день менструального цикла у женщин, когда половая система находится в фолликулярной фазе. Для того чтобы результат был максимально точным, перед анализом ФСГ у женщин необходимо:
- сдавать анализ утром, натощак;
- не принимать гормональных препаратов в течение двух суток;
- исключить физические и эмоциональные перенапряжения;
- исключить поступление никотина перед тем как сдавать анализ на гормон ФСГ.
При проведении анализа биоматериал берется внутривенно, а непосредственно для определения концентрации ФСГ и ЛГ используется сыворотка крови. Если соблюдать рекомендации лечащего врача, то результаты обследования будут объективными и позволят определить тип гормонального нарушения, чтобы затем начать его эффективное лечение.
Уровень ФСГ и ЛГ: норма и отклонения
Получение результата исследования крови, зачастую, доступно уже на следующий день. На протяжении месячного цикла может изменяться и уровень ФСГ, норма у женщин в то или иное время составляет:
На протяжении месячного цикла может изменяться и уровень ФСГ, норма у женщин в то или иное время составляет:
- лютеиновая фаза — 1,2–9 мЕд/л;
- фолликулярная фаза — 2,8–11,3 мЕд/л;
- овуляторная фаза — 5,8–21 мЕд/л.
В отличие от того, как изменяется ФСГ гормон, норма у женщин может дать полную картину о гормональном состоянии организма. Если же полученные данные не отвечают представленным данным, то женщина может отмечать такую симптоматику:
- скудная менструация;
- нарушение цикла;
- отсутствие овуляции;
- бесплодие;
- лишний вес;
- нарушение функции гипофиза;
- ускоренный рост волос на теле и пр.
Следует сказать, что для женщин, уже прошедших через менопаузу, ФСГ гормон повышен постоянно. Такое явление связано с дисфункцией яичников и прочими возрастно-гормональными изменениями организма.
Когда необходимо пройти анализ на ФСГ, когда сдавать кровь определяет лечащий врач в зависимости от индивидуальных биометрических показателей организма.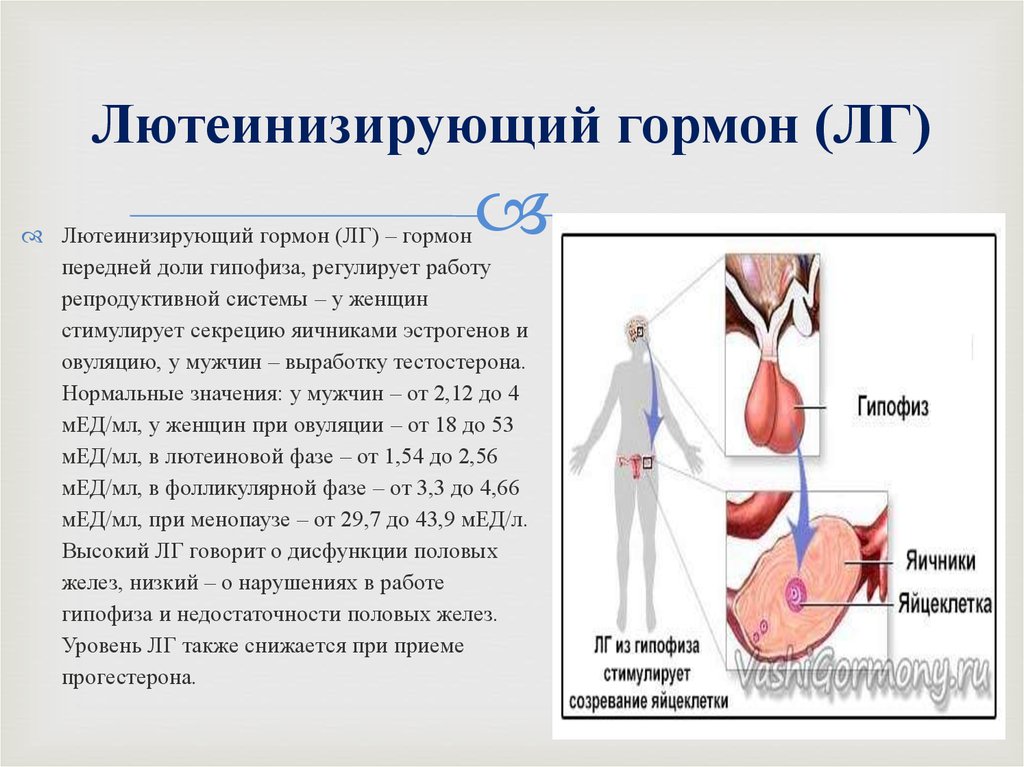 Однако не только это вещество отвечает за репродуктивную функцию. Фертильность определяет отношение ФСГ и ЛГ. Норма соотношения этих показателей в крови сильно варьируется в течение жизни. Так, например, в период полового созревания это 1:1, а в дальнейшем – уже 1:2. Если же коэффициент ФСГ: ЛГ: пролактин находится в приделах 2.5, то это может говорить о:
Однако не только это вещество отвечает за репродуктивную функцию. Фертильность определяет отношение ФСГ и ЛГ. Норма соотношения этих показателей в крови сильно варьируется в течение жизни. Так, например, в период полового созревания это 1:1, а в дальнейшем – уже 1:2. Если же коэффициент ФСГ: ЛГ: пролактин находится в приделах 2.5, то это может говорить о:
- истощении яичников;
- поликистозе яичников;
- опухоли гипофиза и прочих серьезных заболеваниях, вызывающих гормональные сбои.
Как известно, даже если повышен ЛГ и ФСГ, особенно у молодой женщины, это отнюдь не означает невозможность зачатия ребенка. В таком случае допустимо медикаментозно-гормональное воздействие, чтобы в дальнейшем стало возможным провести ЭКО с собственной яйцеклеткой. Отмечается, что ФРГ значительно увеличивается пропорционально уменьшению овариального резерва.
Поэтому при обнаружении подобных проблем со здоровьем, не следует откладывать лечение. Зачастую, в рамках обследований перед ЭКО и для излечения бесплодия проводится фолликулометрия. Когда делать процедуру определит специалист, опираясь на данные о динамике менструального цикла. Такое обследование безболезненно и проводится довольно быстро.
Когда делать процедуру определит специалист, опираясь на данные о динамике менструального цикла. Такое обследование безболезненно и проводится довольно быстро.
Почему анализ на ЛГ, ФСГ, эстрадиол следует сдавать в нашем центре?
Наш медицинский центр специализируется на лечение бесплодия различной природы. Ежегодно мы помогаем стать родителями сотням счастливых семей. У нас можно провести не только анализ ФСГ, но и прочие обследования, которые помогут докторам понять состояние вашей репродуктивной системы и назначить действенное лечение.
Когда повышен ФСГ гормон, норма которого была рассчитана для конкретных возрастно-биометрических показателей, наши специалисты в клинике Центр ЭКО в Тамбове помогут вам справиться с данным синдромом. Мы проводим комплексные обследования обоих партнеров, чтобы понять, что в конкретном случае препятствует естественному оплодотворению и вынашиванию беременности. Для этого достаточно просто записаться на консультацию по одному из номеров, представленных на нашем сайте.
ФСГ (фолликулостимулирующий гормон) — Репродуктивная медицина, гинекология, наблюдение беременности, урология
Фолликулостимулирующий гормон – биоактивное вещество, синтезируемое базофильными клетками аденогипофиза. Наряду с лютеинезирующим (ЛГ) гормоном является гонадотропином, активность которого регулирует гонадолиберин (ГнРГ) гипоталамуса. Продукция ГнРГ характеризуется пульсативной активностью, что и обуславливает импульсный механизм синтеза ФСГ.
Краткая характеристика ФСГ
Гормон ФСГ образует комплексы с рецепторами на цитоплазматических мембранах органов-мишеней – яичниках и яичках. Взаимодействуя с рецепторами яичников, ФСГ стимулирует рост и созревание фолликулов, и синтез эстрогенов. В яичках гормон проникает через гаметотестикулярный барьер и активирует процесс сперматогенеза.
При недостаточной функции ФСГ у женщин отмечается:
- задержка роста;
- снижается скорость формирования и созревания фолликулов;
- медленнее формируются вторичные половые признаки, в том числе задерживается рост молочных желез;
- бесплодие.

У мужчин происходит:
- задержка физического и умственного развития;
- недоразвитие внутренних и наружных половых желез;
- снижается воздействие на деление клеток Лейдинга и выработку тестостерона;
- уменьшается синтез ингибина;
- снижение сперматогенеза;
- замедленное формирование вторичных половых признаков;
- снижение сексуального влечения.
Когда необходимо сдавать анализ
У женщин назначают анализ на ФСГ при:
- бесплодии;
- нарушениях процесса образования фолликулов;
- неоднократном самопроизвольном прерывании беременности;
- сбоях менструального цикла;
- маточных кровотечениях;
- патологиях репродуктивной системы;
- недостаточности половых желез;
- множественных кистах в яичниках.
У мужчин при:
- импотенции;
- нарушении сперматогенеза, особенно олигоспермия и азооспермия;
- снижении или отсутствии либидо;
- бесплодии;
- недостаточности половых желез.

Норма гормона ФСГ отличается у представителей разных полов, а у женского пола определяется еще и фазой цикла. Чтобы определить количество ФСГ, проводят анализ венозной крови. Мужчинам время, когда сдавать материал для исследования, не привязывается к циркадным изменениям.
У женщин существуют наиболее благоприятные дни – 3-6 день в самом начале месячного цикла и 19-21 в конце. Тем женщинам, у кого цикл нерегулярный, когда и как сдавать анализ, подскажет гинеколог или эндокринолог.
Чтобы получить объективный результат анализа, необходимо действовать по установленному алгоритму.
Правила подготовки к сдаче материала
Кровь нужно сдавать:
- на голодный желудок – не рекомендуется есть за 8-12 ч до анализа;
- утром до 10 ч;
- не употреблять гормональные препараты. Если отменить лекарства нельзя, то предупреждают лаборанта;
- за 1-2 ч нельзя курить;
- за 1-2 дня не выполнять тяжелую работу и не заниматься спортом.

Референсные значения ФСГ зависят от пола и возраста пациента. Норма гормона ФСГ представлена в таблице:
| Пол | Возраст (лет) | Фаза цикла | Норма (мЕД/л) |
| Мужчины | ˂1 | ˂ 3,4 | |
| 1-5 | ˂1,42 | ||
| 6-10 | ˂ 3,05 | ||
| 11-14 | 0,35-6,27 | ||
| 15-20 | 0,47-10 | ||
| ˃ 21 | 0,96 – 13,5 | ||
| Женщины | |||
| фолликулярная | 2,7-10,5 | ||
| овулярная | 5,5-29,5 | ||
| лютеиновая | 1,7-6,5 | ||
| менопауза | 37,0-100,0 |
Во время беременности ФСГ низкий. Фоллитропин может быть понижен при:
Фоллитропин может быть понижен при:
- вторичной форме гипогонадизма;
- гипоталамусной гипофункции;
- анорексии невротического характера;
- серповидной анемии;
- опухоли простаты и яичников;
- гемохроматозе.
Повышен ФСГ в период менопаузы, а также высокий показатель характерен при таких заболеваниях:
- первичный тип гипогонадизма;
- синдром Тернера;
- алкогольная зависимость;
- агенезия тестикул или яичников;
- синдром Клайнфельтера;
- кастрация.
Если фоллитропин выше нормы, то назначают дополнительные исследования. Цена исследования в Киеве разная. В разных регионах Украины стоимость исследования колеблется.
Врачи медцентра
Данкович
Наталия Александровна
Акушер-гинеколог, репродуктолог
Котлик
Владимир Владимирович
Акушер-гинеколог, репродуктолог
Каверина
Виктория Алексеевна
Акушер-гинеколог, репродуктолог
Холодян
Ирина Ярославовна
Акушер-гинеколог, репродуктолог, врач ультразвуковой диагностики
Малова
Юлия Александровна
Акушер-гинеколог, гинеколог-эндокринолог, репродуктолог
Гришай
Галина Сергеевна
Акушер-гинеколог
Физиология, Фолликулостимулирующий гормон — StatPearls
Мишель Орловски; Манбир С. Сарао.
Сарао.
Информация об авторе и сведения о членстве
Последнее обновление: 8 мая 2022 г.
Введение
Фолликулостимулирующий гормон (ФСГ) — это гормон, вырабатываемый передней долей гипофиза в ответ на гонадотропин-рилизинг-гормон (ГнРГ) из гипоталамуса. [1]
ФСГ играет роль в половом развитии и репродукции как мужчин, так и женщин.
Проблемы, вызывающие озабоченность
Фертильность
Половое развитие
Аменорея
Менопауза 9 0003
Аденомы гипофиза
Клеточный уровень
ФСГ представляет собой димер гликопротеина с альфа- и бета-субъединицами. Бета-субъединица уникальна для ФСГ, а альфа-субъединица такая же, как у ТТГ, ХГЧ и ЛГ. [2]
ГнРГ стимулирует высвобождение ФСГ. Гипоталамус продуцирует ГнРГ, и он высвобождается в гипофизарную портальную циркуляцию, чтобы воздействовать на рецепторы, связанные с G-белком, в гонадотропных клетках передней доли гипофиза. Эти гонадотропные клетки продуцируют ФСГ и лютеинизирующий гормон (ЛГ) и выделяют их в периферический кровоток.
Эти гонадотропные клетки продуцируют ФСГ и лютеинизирующий гормон (ЛГ) и выделяют их в периферический кровоток.
Высвобождение ГнРГ происходит пульсирующим образом, при этом низкие частоты импульсов стимулируют большую выработку ФСГ, а высокие частоты импульсов стимулируют большую выработку ЛГ.[1] Непрерывное использование ГнРГ подавляет высвобождение ФСГ и ЛГ из передней доли гипофиза, что подавляет овуляцию и выработку эстрогена у женщин. Клинически агонисты ГнРГ, такие как лейпролид, работают по этому механизму.[3]
У женщин отрицательная обратная связь от уровня эстрогена подавляет секрецию ФСГ.[4] У мужчин уровни ингибина B, секретируемого клетками Сертоли в ответ на ФСГ, ингибируют секрецию ФСГ посредством отрицательной обратной связи.[5]
Развитие
Во время внутриутробного развития нейроны, продуцирующие ГнРГ, развиваются из эпителия медиальной обонятельной ямки и затем мигрируют в гипоталамус.[6] Передняя доля гипофиза развивается из кармана Ратке, части ротовой полости. [2]
[2]
Во втором и третьем триместрах беременности, а также в течение первых 3–6 месяцев грудного возраста гипофиз секретирует ЛГ и ФСГ.[7] Уровни ЛГ и ФСГ достигают пика в середине беременности, когда созревает первый фолликул яичника или семявыносящий каналец [6].
У мужчин ФСГ стимулирует пролиферацию клеток Сертоли, которые вносят наибольший вклад в увеличение объема яичек у детей.[7] Клетки Сертоли продуцируют антимюллеров гормон (АМГ), который вызывает инволюцию мюллеровых протоков, предотвращая формирование женских внутренних половых органов.[6]
Клиническая корреляция всплеска ЛГ и ФСГ в раннем младенчестве:
Отсутствие нормального пика ЛГ и ФСГ в младенчестве может выявить и диагностировать у младенцев, особенно мальчиков, гипогонадотропный гипогонадизм.
У девочек с моносомией синдрома Тернера (45, XO) повышение ФСГ до 6 лет связано с отсутствием отрицательной обратной связи от нефункционирующих яичников, а у девочек с мозаицизмом (45, X/46, XX) значительно более низкий уровень ФСГ из-за частичной функции яичников.
 [6]
[6]
В период полового созревания гипоталамус пульсирующим образом секретирует ГнРГ, что стимулирует переднюю долю гипофиза к увеличению секреции ЛГ и ФСГ.[6]
Вовлеченные системы органов
Гипоталамо-гипофизарно-гонадная ось
Гипоталамус секретирует ГнРГ, который стимулирует переднюю долю гипофиза к высвобождению ФСГ и ЛГ. У самок рецепторы ФСГ расположены в гранулезных клетках яичников. У мужчин рецепторы ФСГ обнаружены в клетках Сертоли семенников.[2]
Функция
Самки
Кобели
Механизм
Самки
Производство эстрогена
ФСГ стимулирует клетки гранулезы в фолликулах яичников к синтезу ароматазы, которая превращает андрогены, продуцируемые тека-клетками, в эстрадиол.
Развитие фолликулов и менструальный цикл
Во время фолликулярной фазы менструального цикла ФСГ стимулирует созревание фолликулов яичников. Когда доминантный фолликул берет верх и секретирует эстрадиол и ингибин, секреция ФСГ подавляется. Когда доминантный фолликул вырабатывает достаточное количество эстрадиола для поддержания уровня от 200 до 300 пг/мл в течение 48 часов, гипоталамус реагирует выбросом ГнРГ, который стимулирует секрецию гонадотропных гормонов, а не подавляет их. Пик ФСГ совпадает с пиком ЛГ, вызывающим овуляцию. Затем ФСГ остается низким на протяжении всей лютеиновой фазы, предотвращая развитие новых фолликулов.[2]
Когда доминантный фолликул берет верх и секретирует эстрадиол и ингибин, секреция ФСГ подавляется. Когда доминантный фолликул вырабатывает достаточное количество эстрадиола для поддержания уровня от 200 до 300 пг/мл в течение 48 часов, гипоталамус реагирует выбросом ГнРГ, который стимулирует секрецию гонадотропных гормонов, а не подавляет их. Пик ФСГ совпадает с пиком ЛГ, вызывающим овуляцию. Затем ФСГ остается низким на протяжении всей лютеиновой фазы, предотвращая развитие новых фолликулов.[2]
Кобели
ФСГ вместе с тестостероном необходим для поддержания нормального количества и функции сперматозоидов. Исследования показали, что депривация ФСГ не только снижает количество сперматозоидов, но и влияет на качество оставшейся спермы. [8]
Патофизиология
Повышенные уровни ФСГ связаны с невосприимчивостью гонад или гиперфункцией аденом гипофиза. Низкий уровень ФСГ связан с дисфункцией гипоталамуса или передней доли гипофиза.
Клиническое значение
Уровни ФСГ и
Мужское бесплодие
Если у мужчин имеются маленькие твердые яички и азооспермия или олигоспермия, повышенные уровни ФСГ можно использовать для дифференциации синдрома Клайнфельтера от гипоталамической или гипофизарной недостаточности. Если размер яичек нормальный и у пациентов имеется азооспермия или олигоспермия, уровни ФСГ можно использовать для определения того, является ли причина первичным нарушением сперматогенеза или обструктивным. При обструктивной причине бесплодия уровни ФСГ остаются нормальными, в то время как первичное нарушение сперматогенеза проявляется повышенными уровнями ФСГ.
Если размер яичек нормальный и у пациентов имеется азооспермия или олигоспермия, уровни ФСГ можно использовать для определения того, является ли причина первичным нарушением сперматогенеза или обструктивным. При обструктивной причине бесплодия уровни ФСГ остаются нормальными, в то время как первичное нарушение сперматогенеза проявляется повышенными уровнями ФСГ.
Несколько препаратов ФСГ использовались для лечения вторичного гипогонадизма у мужчин. Эти препараты были достаточно успешными для индукции сперматогенеза и установления отцовства. [8]
Синдром поликистозных яичников
Синдром поликистозных яичников (СПКЯ) представляет собой синдром, характеризующийся повышенным уровнем андрогенов, поликистозными яичниками и ановуляцией. Пациенты с СПКЯ часто имеют гирсутизм, ожирение, резистентность к инсулину, нарушение менструального цикла и бесплодие [9].]
При СПКЯ соотношение ЛГ:ФСГ искажено из-за постоянно частых импульсов ГнРГ. Эти импульсы ГнРГ приводят к увеличению соотношения ЛГ: ФСГ. Это искаженное соотношение приводит к тому, что тека-клетки яичников продуцируют избыток андрогена, в то время как гранулёзные клетки не продуцируют достаточное количество ароматазы для преобразования андрогенов в эстрадиол.
Это искаженное соотношение приводит к тому, что тека-клетки яичников продуцируют избыток андрогена, в то время как гранулёзные клетки не продуцируют достаточное количество ароматазы для преобразования андрогенов в эстрадиол.
Гипогонадотропный гипогонадизм
В случаях аменореи с низким уровнем ФСГ и ЛГ вина лежит либо на гипоталамусе, либо на гипофизе.
Стресс-индуцированный
Гипогонадотропный гипогонадизм
Когда потребление калорий меньше расхода энергии, физиологический стресс снижает частоту и амплитуду импульсов гипоталамического ГнРГ, что приводит к снижению уровней ФСГ и ЛГ. Это объясняет ановуляцию и аменорею, которые могут возникнуть у спортсменок и людей с расстройствами пищевого поведения из-за недостаточного потребления калорий или чрезмерных физических упражнений.
Синдром Каллмана
Во время внутриутробного развития нейроны гипоталамуса, продуцирующие ГнРГ, развиваются из эпителия медиальной обонятельной ямки и затем мигрируют на свое место. [6] При синдроме Каллмана дефект этого миграционного процесса приводит к сочетанию аносмии и гипогонадотропного гипогонадизма.[2]
[6] При синдроме Каллмана дефект этого миграционного процесса приводит к сочетанию аносмии и гипогонадотропного гипогонадизма.[2]
Первичная яичниковая недостаточность
В случаях аменореи с повышенным уровнем ФСГ проблема заключается в яичниках.
Преждевременная недостаточность яичников возникает, когда недостаточность яичников и менопауза наступают в возрасте до 40 лет. Когда это происходит, уровни ФСГ повышаются из-за отсутствия отрицательной обратной связи от яичников. Хотя может быть несколько генетических причин, большинство случаев являются идиопатическими.
Синдром Тернера является наиболее распространенным генетическим заболеванием, вызывающим преждевременную недостаточность яичников. Синдром Тернера вызывается потерей Х-хромосомы (кариотип ХО). У девочек с синдромом Тернера будет первичная аменорея, недоразвитые яичники (полосатые яичники) и повышенный уровень ФСГ.[10]
Аденомы гипофиза
Аденомы гипофиза могут развиваться из любого типа клеток гипофиза. Аденомы гипофиза, происходящие из гонадотропных клеток, чаще всего нефункционируют или функционируют в пределах нормальных уровней гормонов и диагностируются на основании симптомов масс-эффекта, а не секреции гормонов. Однако в спорадических случаях эти опухоли могут секретировать избыток ФСГ и/или ЛГ и вызывать гиперстимуляцию яичников.[11]
Аденомы гипофиза, происходящие из гонадотропных клеток, чаще всего нефункционируют или функционируют в пределах нормальных уровней гормонов и диагностируются на основании симптомов масс-эффекта, а не секреции гормонов. Однако в спорадических случаях эти опухоли могут секретировать избыток ФСГ и/или ЛГ и вызывать гиперстимуляцию яичников.[11]
Лекарства
Агонисты и антагонисты ГнРГ
Агонисты ГнРГ первоначально стимулируют секрецию ЛГ и ФСГ, но при длительном введении подавляют высвобождение ЛГ и ФСГ. Это приводит к подавлению яичников и снижению уровня эстрогена. Антагонисты ГнРГ могут резко подавлять секрецию ЛГ и ФСГ.[2]
Как агонисты, так и антагонисты ГнРГ играют важную роль в лечении некоторых видов рака молочной железы и предстательной железы, эндометриоза и лейомиомы матки.
Методы вспомогательной репродукции (ВРТ)
Такие методы, как экстракорпоральное оплодотворение (ЭКО) и интрацитоплазматическая инъекция сперматозоидов (ИКСИ), помогают парам использовать ФСГ для стимуляции нескольких фолликулов в яичниках для сбора нескольких яйцеклеток для оплодотворения. ФСГ доступен в виде ФСГ в моче с ЛГ или без него или рекомбинантного ФСГ.[12] Агонисты или антагонисты ГнРГ могут использоваться во время этих циклов для предотвращения всплеска ЛГ и овуляции.[2]
ФСГ доступен в виде ФСГ в моче с ЛГ или без него или рекомбинантного ФСГ.[12] Агонисты или антагонисты ГнРГ могут использоваться во время этих циклов для предотвращения всплеска ЛГ и овуляции.[2]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Stamatiades GA, Kaiser UB. Регуляция гонадотропина пульсирующим GnRH: передача сигналов и экспрессия генов. Мол Селл Эндокринол. 2018 05 марта; 463: 131-141. [Бесплатная статья PMC: PMC5812824] [PubMed: 29102564]
- 2.
Barbieri RL. Эндокринология менструального цикла. Методы Мол Биол. 2014;1154:145-69. [PubMed: 24782009]
- 3.
Йонкерс К.А., Симони М.К. Предменструальные расстройства. Am J Obstet Gynecol. 2018 Январь; 218(1):68-74. [PubMed: 28571724]
- 4.
Shaw ND, Histed SN, Srouji SS, Yang J, Lee H, Hall JE.
 Отрицательная обратная связь эстрогена с секрецией гонадотропина: свидетельство прямого гипофизарного эффекта у женщин. J Clin Endocrinol Metab. 2010 Апрель; 95 (4): 1955-61. [Бесплатная статья PMC: PMC2853991] [PubMed: 20133465]
Отрицательная обратная связь эстрогена с секрецией гонадотропина: свидетельство прямого гипофизарного эффекта у женщин. J Clin Endocrinol Metab. 2010 Апрель; 95 (4): 1955-61. [Бесплатная статья PMC: PMC2853991] [PubMed: 20133465]- 5.
Boepple PA, Hayes FJ, Dwyer AA, Raivio T, Lee H, Crowley WF, Piteloud N. Относительная роль ингибина B и половых стероидов в регуляции отрицательной обратной связи фолликулостимулирующего гормона у мужчин во всем спектре семенного эпителия функция. J Clin Endocrinol Metab. 2008 май; 93 (5): 1809-14. [PMC free article: PMC2386680] [PubMed: 18270253]
- 6.
Lanciotti L, Cofini M, Leonardi A, Penta L, Esposito S. Обзор Minipuber и overview на гипотеал. Активация гонадной оси в жизни плода и новорожденного. Фронт Эндокринол (Лозанна). 2018;9:410. [Бесплатная статья PMC: PMC6070773] [PubMed: 30093882]
- 7.
Grinspon RP, Urrutia M, Rey RA. Мужской центральный гипогонадизм в педиатрии — актуальность фолликулостимулирующего гормона и маркеров клеток Сертоли.
 Евро Эндокринол. 2018 сен;14(2):67-71. [Бесплатная статья PMC: PMC6182919] [PubMed: 30349597]
Евро Эндокринол. 2018 сен;14(2):67-71. [Бесплатная статья PMC: PMC6182919] [PubMed: 30349597]- 8.
Нишлаг Э., Симони М., Громолл Дж., Вайнбауэр Г.Ф. Роль ФСГ в регуляции сперматогенеза: клинические аспекты. Клин Эндокринол (Oxf). 1999 августа; 51(2):139-46. [PubMed: 10468980]
- 9.
Кришнан А., Мутусами С. Гормональные изменения при СПКЯ и их влияние на метаболизм костей. J Эндокринол. 2017 февраль; 232(2):R99-R113. [PubMed: 27895088]
- 10.
Pouresmaeili F, Fazeli Z. Преждевременная недостаточность яичников: критическое состояние репродуктивного потенциала с различными генетическими причинами. Int J Fertil Steril. 2014 апр;8(1):1-12. [Бесплатная статья PMC: PMC3973172] [PubMed: 24696764]
- 11.
Кихара М., Сугита Т., Нагаи Ю., Саэки Н., Тацуно И., Секи К. Гиперстимуляция яичников, вызванная аденомой гонадотропных клеток: отчет о клиническом случае и обзор литературы. Гинекол Эндокринол.
 2006 февраля; 22 (2): 110-3. [PubMed: 16603438]
2006 февраля; 22 (2): 110-3. [PubMed: 16603438]- 12.
Pouwer AW, Farquhar C, Kremer JA. ФСГ пролонгированного действия по сравнению с суточной дозой ФСГ у женщин, перенесших вспомогательную репродукцию. Cochrane Database Syst Rev. 2015 Jul 14;(7):CD009577. [PubMed: 26171903]
Мужской гипогонадизм | Вы и ваши гормоны от Общества эндокринологов
Альтернативные названия мужского гипогонадизма
Синдром дефицита тестостерона; дефицит тестостерона; первичный гипогонадизм; вторичный гипогонадизм; гипергонадотропный гипогонадизм; гипогонадотропный гипогонадизм
Что такое мужской гипогонадизм?
Мужской гипогонадизм описывает состояние низкого уровня мужского гормона тестостерона у мужчин. Тестостерон вырабатывается в яичках, и он важен для развития мужских характеристик, таких как огрубление голоса, рост волос на лице и лобке, а также рост полового члена и яичек в период полового созревания. В гипоталамусе кисспептин вызывает высвобождение гонадотропин-высвобождающего гормона, который, в свою очередь, стимулирует гипофиз к выработке лютеинизирующего гормона и фолликулостимулирующего гормона (гонадотропинов).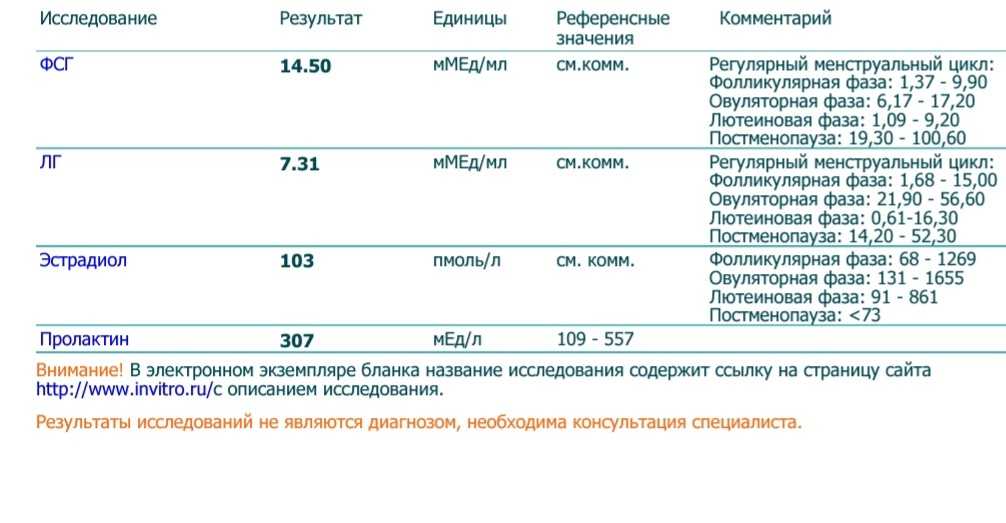 Затем гонадотропины воздействуют на яички, заставляя их вырабатывать тестостерон. Низкий уровень тестостерона может возникать из-за заболеваний яичек или состояний, влияющих на гипоталамус или гипофиз. Мужчины могут быть поражены в любом возрасте и проявлять различные симптомы в зависимости от времени заболевания по отношению к началу полового созревания. В некоторых случаях может быть трудно сказать, существует ли истинный дефицит тестостерона, особенно когда его уровень находится в пограничном диапазоне.
Затем гонадотропины воздействуют на яички, заставляя их вырабатывать тестостерон. Низкий уровень тестостерона может возникать из-за заболеваний яичек или состояний, влияющих на гипоталамус или гипофиз. Мужчины могут быть поражены в любом возрасте и проявлять различные симптомы в зависимости от времени заболевания по отношению к началу полового созревания. В некоторых случаях может быть трудно сказать, существует ли истинный дефицит тестостерона, особенно когда его уровень находится в пограничном диапазоне.
Что вызывает мужской гипогонадизм?
Мужской гипогонадизм можно разделить на две группы. Классический гипогонадизм — это когда низкий уровень тестостерона вызван основным конкретным заболеванием, например, синдромом Клайнфельтера, синдромом Каллмана или опухолью гипофиза. Поздний гипогонадизм — это когда снижение уровня тестостерона связано с общим старением и/или возрастными заболеваниями. Кроме того, ожирение и диабет 2 типа могут быть связаны с гипогонадизмом у мужчин.
Классический мужской гипогонадизм бывает двух видов – первичный и вторичный. Первичный гипогонадизм возникает, когда низкий уровень тестостерона обусловлен состояниями, поражающими яички. Первичный гипогонадизм также называют гипергонадотропным гипогонадизмом, при котором гипофиз вырабатывает слишком много лютеинизирующего гормона (ЛГ) и фолликулостимулирующего гормона (ФСГ) (гонадотропины), чтобы попытаться стимулировать яички для производства большего количества тестостерона. Однако, поскольку яички повреждены или отсутствуют, они не способны реагировать на повышенный уровень гонадотропинов, и тестостерон вырабатывается в малом количестве или вообще не вырабатывается. У некоторых пациентов с первичным гипогонадизмом уровни тестостерона могут быть в пределах нормы, но повышенные ЛГ и ФСГ указывают на то, что гипофиз пытается компенсировать дефицит, и лечение все же может потребоваться.
Примеры состояний, поражающих яички, которые приводят к первичной недостаточности половых желез, включают:
- воспаление, вызванное такими инфекциями, как эпидемический паротит
- химиотерапия или лучевая терапия яичек
- неопущение яичек в мошонку
- отсутствие яичек (анорхизм)
- Синдром Клайнфельтера — генетическое заболевание, при котором мужчины рождаются с дополнительной Х-хромосомой; характеризуется высоким ростом, сниженной фертильностью и развитием ткани молочной железы
- некоторые виды опухолей
- некоторые виды аутоиммунных заболеваний
Вторичный гипогонадизм возникает, когда передача сигналов яичкам неспособна стимулировать достаточную выработку тестостерона и вызвана состояниями, влияющими на функцию гипоталамуса и/или гипофиза. Он также известен как гипогонадотропный гипогонадизм из-за низкого уровня ЛГ и ФСГ, что приводит к снижению выработки тестостерона. Вторичный гипогонадизм часто возникает как часть более широкого синдрома гипопитуитаризма. Примеры причин могут включать:
Он также известен как гипогонадотропный гипогонадизм из-за низкого уровня ЛГ и ФСГ, что приводит к снижению выработки тестостерона. Вторичный гипогонадизм часто возникает как часть более широкого синдрома гипопитуитаризма. Примеры причин могут включать:
- опухоли гипофиза и их лечение
- изолированный гипогонадотропный гипогонадизм (низкий уровень гонадотропин-рилизинг-гормона с рождения)
- Синдром Каллмана — редкое генетическое заболевание, которое вызывает остановку развития нервных клеток в гипоталамусе, вырабатывающих гонадотропин-высвобождающий гормон. Это приводит к неспособности пройти половое созревание, потере полового созревания и неспособности развиваться яичкам. Обычно это связано с потерей обоняния.
- употребление анаболических стероидов
- Синдром Прадера-Вилли
- травма головы.
Каковы признаки и симптомы мужского гипогонадизма?
Признаки и симптомы зависят от стадии, на которой у пациента проявляется гипогонадизм по отношению к половой зрелости. Если дефицит тестостерона возникает до или во время полового созревания, признаки и симптомы могут включать:
Если дефицит тестостерона возникает до или во время полового созревания, признаки и симптомы могут включать:
- Задержка полового созревания:
- отсутствие развития яичек и отсутствие роста полового члена
- отсутствие волос на лобке и лице
- отказ голоса сломаться
- снижение или отсутствие выработки сперматозоидов в яичках, что приводит к бесплодию.
- Замедленный костный возраст (когда зрелость скелета отстает от вашего возраста в годах).
В период полового созревания мальчики со слишком низким уровнем тестостерона также могут иметь меньшую, чем обычно, силу и выносливость, а их руки и ноги могут продолжать расти непропорционально остальным частям тела.
У мужчин, которые уже достигли половой зрелости, симптомы могут включать:
- неадекватную эрекцию, потерю либидо и плохую сексуальную активность
- усталость
- потеря мотивации и концентрации
- выпадение волос на лобке и лице
- снижение количества сперматозоидов
- мягкие, маленькие яички
- изменения настроения
- увеличение жировых отложений
- разрастание ткани молочной железы (гинекомастия)
- истончение костей (остеопороз)
- снижение мышечной массы и физической силы
- морщинистая «пергаментная» кожа
- повышенное потоотделение.

Поскольку некоторые из этих симптомов (например, усталость, изменения настроения) могут быть вызваны несколькими причинами, диагноз мужского гипогонадизма иногда может быть изначально пропущен.
Насколько распространен мужской гипогонадизм?
Мужской гипогонадизм чаще встречается у стареющих мужчин. Уровень тестостерона у мужчин начинает падать после 40 лет. Было подсчитано, что 8,4% мужчин в возрасте 50–79 летлет имеют дефицит тестостерона. Мужской гипогонадизм также связан с диабетом 2 типа: по оценкам, примерно у 17 % мужчин с диабетом 2 типа низкий уровень тестостерона.
Наследуется ли мужской гипогонадизм?
Мужской гипогонадизм не передается по наследству. Существуют генетические причины гипогонадизма, к которым относятся синдром Клайнфельтера и синдром Каллмана; однако эти состояния возникают спорадически, они не наследуются от родителей.
Как диагностируется мужской гипогонадизм?
Необходимо собрать подробный анамнез. В частности, важно выяснить, была ли завершена вирилизация (развитие нормальных мужских признаков) при рождении, опустились ли яички, и посмотреть, прошел ли период полового созревания пациента в то же время, что и его сверстники. Пациента следует тщательно обследовать и зафиксировать наличие и размер яичек, а также правильность их положения в мошонке.
В частности, важно выяснить, была ли завершена вирилизация (развитие нормальных мужских признаков) при рождении, опустились ли яички, и посмотреть, прошел ли период полового созревания пациента в то же время, что и его сверстники. Пациента следует тщательно обследовать и зафиксировать наличие и размер яичек, а также правильность их положения в мошонке.
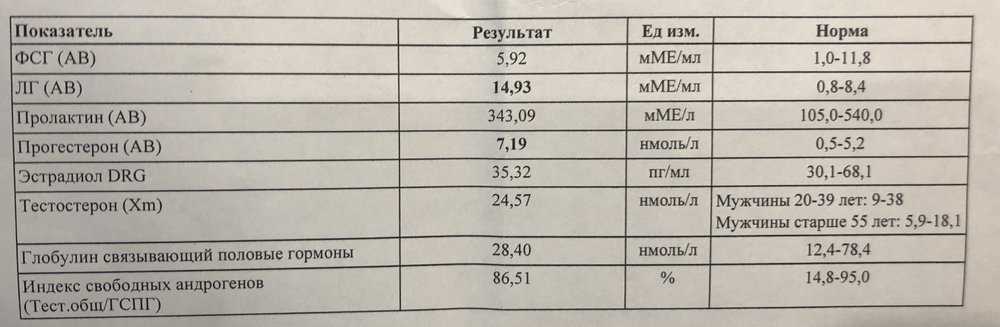
Многие симптомы мужского гипогонадизма неспецифичны и могут быть вызваны целым рядом состояний. Поэтому при диагностике гипогонадизма важно проводить биохимические тесты для оценки уровня тестостерона в крови для подтверждения диагноза. Будут проведены анализы крови для измерения уровня тестостерона. Образец крови следует собирать утром между 08:00 и 10:00, когда уровень тестостерона самый высокий (поскольку уровни тестостерона меняются в течение дня) и натощак (поскольку прием пищи может снизить уровень тестостерона). Анализ крови может проводиться амбулаторно. Если результат первого теста показывает низкий уровень тестостерона, тест следует повторить через две-три недели для подтверждения результата. Другие гормоны также тестируются вместе со вторым образцом крови. Эти гормоны включают лютеинизирующий гормон, фолликулостимулирующий гормон и пролактин (вырабатывается гипофизом). Результаты этих анализов крови помогут отличить первичный (низкий уровень тестостерона и высокий уровень гонадотропинов) и вторичный (низкий уровень тестостерона и нормальный или низкий уровень гонадотропинов) гипогонадизм. Тестостерон переносится кровотоком с помощью белка, называемого глобулином, связывающим половые гормоны (ГСПГ). ГСПГ часто проверяют одновременно с тестостероном, поскольку это облегчает интерпретацию наличия истинного дефицита. У пациентов с ожирением и сахарным диабетом 2 типа уровень ГСПГ часто бывает низким, из-за чего уровень тестостерона может казаться ниже, чем он есть на самом деле.
Другие гормоны также тестируются вместе со вторым образцом крови. Эти гормоны включают лютеинизирующий гормон, фолликулостимулирующий гормон и пролактин (вырабатывается гипофизом). Результаты этих анализов крови помогут отличить первичный (низкий уровень тестостерона и высокий уровень гонадотропинов) и вторичный (низкий уровень тестостерона и нормальный или низкий уровень гонадотропинов) гипогонадизм. Тестостерон переносится кровотоком с помощью белка, называемого глобулином, связывающим половые гормоны (ГСПГ). ГСПГ часто проверяют одновременно с тестостероном, поскольку это облегчает интерпретацию наличия истинного дефицита. У пациентов с ожирением и сахарным диабетом 2 типа уровень ГСПГ часто бывает низким, из-за чего уровень тестостерона может казаться ниже, чем он есть на самом деле.
В зависимости от результатов вышеуказанных тестов могут быть проведены другие исследования. К ним относятся: сканирование плотности костей для оценки влияния дефицита тестостерона на кости; анализ спермы; генетические исследования; УЗИ яичек, чтобы проверить наличие узелков или новообразований; и МРТ гипофиза.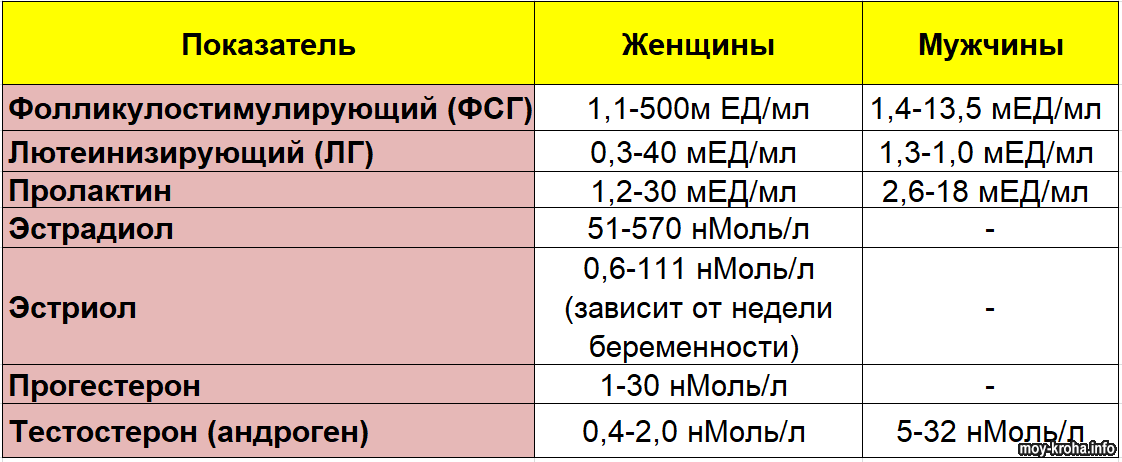
Как лечить мужской гипогонадизм?
Лечение классического гипогонадизма включает заместительную терапию тестостероном с целью повышения уровня тестостерона в крови до нормального уровня. Точное лечение будет варьироваться между пациентами и будет адаптировано к их индивидуальным потребностям. Доступны различные препараты тестостерона:
- Инъекционные формы – это препараты, которые можно вводить в мышцы либо каждые три-четыре недели, либо каждые три месяца.
- Ежедневное (утреннее) нанесение геля тестостерона на кожу.
- Имплантаты тестостерона – небольшие гранулы, помещаемые под кожу. Их все чаще заменяют трехмесячными инъекциями тестостерона.
Все эти варианты следует обсудить с врачом и выбрать наиболее подходящий вариант лечения. Во время лечения заместительной терапией тестостероном следует проводить регулярные анализы крови для контроля уровня тестостерона и, при необходимости, корректировать дозу, чтобы гарантировать, что уровни возвращаются к нормальному диапазону. Таблетированные формы тестостерона, принимаемые внутрь, не рекомендуются из-за связи с повреждением печени, а также из-за того, что сложнее контролировать замену.
Таблетированные формы тестостерона, принимаемые внутрь, не рекомендуются из-за связи с повреждением печени, а также из-за того, что сложнее контролировать замену.
Тестостерон не следует назначать, если у пациента рак предстательной железы, поскольку это может привести к более быстрому росту опухоли. Перед началом лечения тестостероном проводится анализ крови для измерения гормона, вырабатываемого предстательной железой, который называется ПСА (специфический антиген простаты) (уровень ПСА повышен при раке предстательной железы). Предстательную железу также можно обследовать (через задний проход), чтобы исключить рак предстательной железы.
Для пациентов, у которых был диагностирован гипогонадизм с поздним началом, в настоящее время недостаточно доказательств, чтобы мы знали, является ли лечение тестостероном безопасным и эффективным в долгосрочной перспективе. Несмотря на то, что есть некоторые краткосрочные исследования, которые показывают, что он может принести пользу этим пациентам в течение короткого периода времени, существует потребность в более долгосрочных клинических испытаниях в этой области с участием большого числа пациентов для оценки долгосрочного воздействия. Лечение тестостероном пациентов с поздним гипогонадизмом. Области, которые требуют особого внимания, — это оценка воздействия лечения на вероятность развития сердечно-сосудистых заболеваний, рака предстательной железы и вторичной полицитемии (состояние, при котором в крови увеличивается количество эритроцитов, что может предрасполагать к увеличению образования тромбов).
Лечение тестостероном пациентов с поздним гипогонадизмом. Области, которые требуют особого внимания, — это оценка воздействия лечения на вероятность развития сердечно-сосудистых заболеваний, рака предстательной железы и вторичной полицитемии (состояние, при котором в крови увеличивается количество эритроцитов, что может предрасполагать к увеличению образования тромбов).
Если у пациентов есть какие-либо опасения по поводу своего здоровья, им следует в первую очередь обратиться к своему терапевту.
Есть ли у лечения побочные эффекты?
В зависимости от используемой формы заместительная терапия тестостероном может иметь легкие побочные эффекты: инъекционные формы могут вызывать боль и кровоподтеки в месте инъекции; гелеобразная форма может вызвать раздражение кожи.
Лечение тестостероном может вызвать увеличение количества эритроцитов (известное как полицитемия), что увеличивает риск тромбоза. Во время лечения следует проводить регулярные анализы крови, чтобы проверить увеличение количества эритроцитов. Увеличение предстательной железы является еще одним серьезным побочным эффектом, который следует контролировать. Обследование предстательной железы и анализ крови на ПСА следует проводить каждые три месяца в течение первого года, а затем ежегодно у мужчин в возрасте старше 40 лет после начала лечения. Если у пациентов есть какие-либо опасения по поводу этих возможных побочных эффектов, им следует обсудить их со своим врачом.
Увеличение предстательной железы является еще одним серьезным побочным эффектом, который следует контролировать. Обследование предстательной железы и анализ крови на ПСА следует проводить каждые три месяца в течение первого года, а затем ежегодно у мужчин в возрасте старше 40 лет после начала лечения. Если у пациентов есть какие-либо опасения по поводу этих возможных побочных эффектов, им следует обсудить их со своим врачом.
Каковы долгосрочные последствия мужского гипогонадизма?
Симптомы мужского гипогонадизма, такие как отсутствие полового влечения, неадекватная эрекция (эректильная дисфункция) и бесплодие, могут приводить к низкой самооценке и вызывать депрессию. Доступны профессиональные консультации, которые помогут справиться с этими побочными эффектами; пациенты должны поговорить со своим врачом для получения дополнительной информации. Пациенты обычно отмечают улучшение полового влечения и самооценки после заместительной терапии тестостероном. Эректильная дисфункция является распространенным симптомом у пациентов без гипогонадизма и может нуждаться в лечении в дополнение к тестостерону./18/18_1.jpg)
Мужской гипогонадизм связан с повышенным риском развития сердечных заболеваний (низкий уровень тестостерона может вызвать повышение уровня холестерина). Исследования показали, что уровень тестостерона может быть ниже у мужчин с диабетом 2 типа и у мужчин с избыточной массой тела. Однако неясно, является ли это ассоциацией или прямой причиной и следствием. Изменения в образе жизни для снижения веса и увеличения количества физических упражнений могут повысить уровень тестостерона у мужчин с диабетом.
Уровень тестостерона у мужчин естественным образом снижается с возрастом. В средствах массовой информации это иногда называют мужской менопаузой (андропаузой), хотя это не общепринятый медицинский термин. Низкий уровень тестостерона также может вызвать трудности с концентрацией внимания, потерю памяти и проблемы со сном. Текущие исследования показывают, что этот эффект наблюдается только у небольшой группы стареющих мужчин. Тем не менее, в настоящее время проводится много исследований, чтобы узнать больше о влиянии тестостерона на пожилых мужчин, а также о том, будет ли использование заместительной терапии тестостероном иметь какие-либо преимущества.





 [6]
[6] Отрицательная обратная связь эстрогена с секрецией гонадотропина: свидетельство прямого гипофизарного эффекта у женщин. J Clin Endocrinol Metab. 2010 Апрель; 95 (4): 1955-61. [Бесплатная статья PMC: PMC2853991] [PubMed: 20133465]
Отрицательная обратная связь эстрогена с секрецией гонадотропина: свидетельство прямого гипофизарного эффекта у женщин. J Clin Endocrinol Metab. 2010 Апрель; 95 (4): 1955-61. [Бесплатная статья PMC: PMC2853991] [PubMed: 20133465] Евро Эндокринол. 2018 сен;14(2):67-71. [Бесплатная статья PMC: PMC6182919] [PubMed: 30349597]
Евро Эндокринол. 2018 сен;14(2):67-71. [Бесплатная статья PMC: PMC6182919] [PubMed: 30349597] 2006 февраля; 22 (2): 110-3. [PubMed: 16603438]
2006 февраля; 22 (2): 110-3. [PubMed: 16603438]